
【题目】某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,均充分反应,实验数据如下:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | |
加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
(1)黄铜样品中锌的质量分数为多少?(写出计算步骤,下同)
(2)所用稀硫酸的质量分数为多少?
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:初中化学 来源: 题型:
【题目】请根据下列各图中有关信息,回答下列问题:
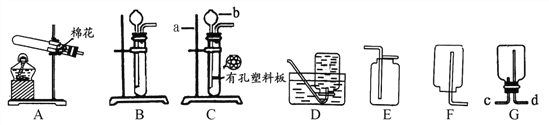
(1)仪器a、b的名称:a________,b________。
(2)若用装置A制取氧气,其反应的化学方程式_______________。若要收集到较纯净的氧气,其收集装置应选____;待收集完毕后应先_______,再________________。 某同学用收集好的氧气做铁丝燃烧实验时发现集气瓶炸裂,原因可能是_________。
(3)实验制取CO2,为了控制反应的发生与停止,选择最佳的发生装置是___________;若用G装置收集CO2气体,气体应从________端(填“c”或“d”)进入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在生产生活中有广泛应用。
(1) 2018年,昆明到大理的高铁开通后,人们的出行将更加方便、快捷,高铁建设需要大量的金属材料。动车电路中使用很多的铜线,这是利用了铜的延展性和_______________________。动车表面喷漆除美观外,主要是为了防止外壳生锈,其防锈的原理是__________________保护金属资源的途径除防止金属的腐蚀外,还有____________________ (答一条)。

(2)生铁和钢都是_________________合金,生铁中含碳量比钢中_________________ (填“高”或“低”)。
(3)向AgNO3溶液中加入一定质量铝和铁的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液。关于该滤渣和滤液有下列四种说法:
①向滤渣中加入稀盐酸,一定有气泡产生
②向滤液中加人稀盐酸,一定有沉淀产生
③滤液中一定含有Fe(NO3)2,可能含有AgNO3
④滤渣中一定没有铝,可能含有银
以上说法中正确的是 _____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从我们的衣食住行到国防科技都离不开化学。请利用所学化学知识回答下列问题:
(1)下列行为能导致空气中PM2.5含量增加的是____________(填字母)。
A 大量使用化石燃料 B 露天焚烧垃圾 C 发展轨道交通,低碳出行
(2)在TiO2作催化剂和光照条件下,水能分解成氢气和氧气,写出该反应的化学方程式___________。
(3)下列属于复合材料的是_______________ (填字母)。
A 聚酰胺(俗称尼龙)
B 铝合金
C 钢筋混凝土
D 玻璃钢
(4)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与____________共同作用的结果。工业上用稀硫酸清除铁锈的化学反应方程式为_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】能源、环境与人类的生活和社会发展密切相关。
(1)目前,人类以化石燃料为主要能源,常见的化石燃料包括煤、石油和_____。
(2)为减少污染、提高煤的利用率,可将其转化为可燃性气体,此过程可认为是碳与水的反应,其微观示意图如下所示:
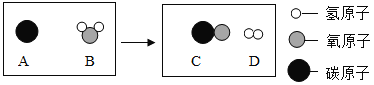
①该反应的基本反应类型为_____。
②该反应生成物的分子个数比为_____。
(3)为减少温室气体排放,人们积极寻找不含碳元素的燃料。经研究发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景。
①NH3中氮元素和氢元素的质量比为_____。
②将NH3燃烧反应的化学方程式补充完整:4NH3+3O2![]() 6H2O+_____。
6H2O+_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请看图回答问题:
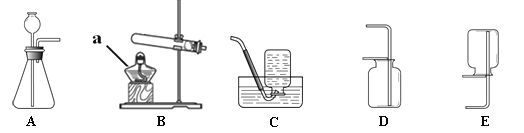
(1)图中仪器a的名称是 。
(2)用B与C相连可以制备 ,该反应的化学方程式为 。
(3)实验室制取二氧化碳应选用的发生装置和收集装置为_______(填序号),选用此收集方法的依据是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法正确的是

A.图中a点所示溶液中,含有的溶质是NaCl和Na0H
B.由a点到b点的pH变化过程证明酸和碱发生了中和反应
C.向图中c点所示溶液中滴加无色酚酞,溶液不变色
D.该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)下列做法中,符合“低碳”理念的是______________(填字母序号)
A 开发使用新能源汽车
B “焚烧法”处理垃圾
C 大力发展火力发电
D 使用太阳能热水器
E 大力发展风力发电
(2)幼儿和青少年缺_________会患佝偻病和发育不良。
(3)如图是A、B、C三种物质的溶解度曲线图。请回答:
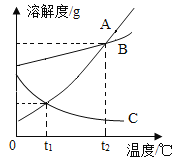
①t1℃时,溶解度相等的两种物质是_____。
②B的饱和溶液中混有少量的物质A,要除去A得到较纯的B物质,可采用的结晶方法是_________________。
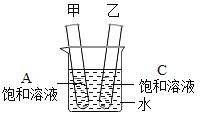
③如图所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是______,乙试管内的溶液为_______溶液(填“饱和”或“不饱和”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】常见金属在氧气中能剧烈燃烧。某化学探究小组对“铁丝在氧气中燃烧为什么会火星四射”有兴趣。于是进行了如下探究:
(提出问题)铁丝在氧气中燃烧会火星四射与哪些因素有关呢?
(猜想与假设)猜想一:可能与金属的沸点有关;猜想二:可能与氧气的浓度有关;猜想三:可能与铁中含碳量有关。
(查阅资料)镁的沸点为1107℃;铁的沸点为2705℃。
(设计并实验)该探究小组用将镁丝、纯细铁丝和两种不同含碳量的细铁丝(镁丝和铁丝直径均为0.4mm)分别放入空气和氧气中燃烧。记录燃烧时的现象如下表。
实验序号 | 氧气纯度(含氧量) | 镁丝 | 铁丝中含碳量 | 燃烧时的现象 |
① | 空气中(21%) | 剧烈燃烧,发出耀眼白光,无火星 | 0%(纯铁) | 不燃烧 |
② | 纯氧中(100%) | 更剧烈燃烧,发出耀眼白光,无火星 | 0%(纯铁) | 剧烈燃烧,无火星 |
③ | 纯氧中(100%) | 更剧烈燃烧,发出耀眼白光,无火星 | 0.05% | 剧烈燃烧,极少火星 |
④ | 纯氧中(100%) | 更剧烈燃烧,发出耀眼白光,无火星 | 0.6% | 剧烈燃烧,火星四射 |
(收集证据)(1)若要比较细铁丝燃烧的剧烈程度与氧气的纯度有关,应选择的实验编号组合是_____。由实验③和④对比可知,产生火星四射的现象与细铁丝中含碳量的关系:_____。
(解释与结论)(2)通过探究,了解细铁丝在纯净的氧气燃烧时会火星四射的原因。请写出细铁丝在氧气中燃烧生成黑色的四氧化三铁固体的化学方程式为:_____。
(3)细铁丝中含有不同的含碳量,碳元素在燃烧过程中生成二氧化碳气体,将反应生成的熔化物四氧化三铁推了出去,从而产生了火星四射的现象。为保证实验成功,选用的铁丝中含碳量要控制的范围为_____。
(4)取一段含碳量0.6%的细铁丝绕成螺旋状,投入盛有足量的稀盐酸的烧杯中充分反应,可观察的现象为_____,并在烧杯底有少量的黑色残渣,其化学式为C。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com