
分析 氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,和氯化钡反应生成碳酸钡沉淀和氯化钠;
稀盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳.
解答 解:加入盐酸的作用是除去过量的氢氧化钠和碳酸钠;
操作③得到的固体成分除了有BaSO4、Mg(OH)2外,还有碳酸钠和氯化钙反应生成的碳酸钙、碳酸钠和氯化钡反应生成的碳酸钡.
故答案为:除去过量的氢氧化钠和碳酸钠;碳酸钙和碳酸钡.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
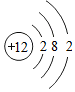 .
.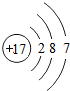 .
.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 万里飘香--分子在不断运动 | B. | 水结成冰--分子本身发生变化 | ||
| C. | 蜡炬成灰--分子质量发生改变 | D. | 轮胎充气--分子大小发生变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
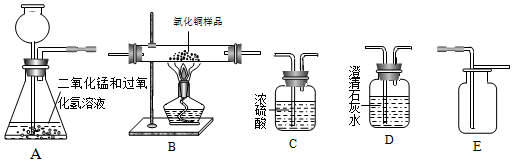
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 禁止使用化肥是防止“水华”的最好方法 | |
| B. | 若使用无磷洗衣粉,可有效防止该藻类的过度生长 | |
| C. | 向河水中过量排放含有氮肥的农田水,也可能造成该藻类的过度生长 | |
| D. | 该藻类由碳、氢、氮、磷4种元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO2、N2 | B. | NO2、O2 | C. | SO2、NO2 | D. | N2、NO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
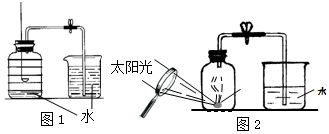 用来测定空气成分的方法很多,图1所示的是小明用红磷在空气中燃烧的测定方法.实验过程是:
用来测定空气成分的方法很多,图1所示的是小明用红磷在空气中燃烧的测定方法.实验过程是:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com