
| A. | N2 | B. | 2N | C. | N | D. | K |
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:初中化学 来源: 题型:选择题

| A. | 甲中①②对比可探究铁的锈蚀与植物油是否有关 | |
| B. | 甲中①③对比可探究铁的锈蚀与水是否有关 | |
| C. | 乙中铜片上的白磷与红磷实验,可探究可燃物的燃烧是否需要与氧气接触 | |
| D. | 乙中铜片上的白磷与热水中的白磷实验,可探究可燃物的燃烧是否需要达到着火点. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
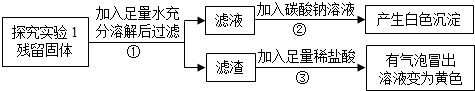
 袋装食品中常用一种“双吸剂”保质,主要成分是铁粉和生石灰,同学们对一久置的双吸剂固体样品很好奇,设计了如下实验进行探究.
袋装食品中常用一种“双吸剂”保质,主要成分是铁粉和生石灰,同学们对一久置的双吸剂固体样品很好奇,设计了如下实验进行探究.| 实验操作 | 实验现象 | 实验结论 |
| 取少量实验探究1的残留固 体放入试管中,加入蒸馏水 | 试管外壁不发烫 | 固体中一定没有氧化钙. |
| 反应时间 | t0 | t1 | t2 | t3 |
| 烧杯和药品的质量/g | 171.5 | 171.3 | 171.1 | 171.1 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
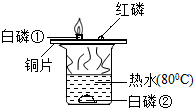 燃烧是我们非常熟悉的化学反应.如图是用实验方法来探究燃烧的条件.(已知:白磷的着火点是40℃,红磷的着火点是240℃).
燃烧是我们非常熟悉的化学反应.如图是用实验方法来探究燃烧的条件.(已知:白磷的着火点是40℃,红磷的着火点是240℃).查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 溶剂的质量一定不变 | B. | 溶质的质量不变 | ||
| C. | 可降低温度或蒸发水分 | D. | 溶液的质量可能不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com