
分析 (1)内燃机的四个冲程分别是:吸气、压缩、做功、排气冲程,此四个冲程为一个工作循环;
(2)根据反应前后元素种类不变,原子个数不变,则可推测X的化学式解答.
解答 解:
(1)汽油机和柴油机工作的四个冲程分别是:吸气、压缩、做功、排气冲程.
(2)根据反应前后元素种类不变,原子个数不变,则:反应前除X外,有碳原子1个、氧原子1个、氮原子2个、氢原子4个;反应后碳原子1个、氮原子2个、氧原子2个、氢原子6个,因此X中有氧原子1个、氢原子2个,故X的化学式是H2O.
答案:
(1)做功;
(2)H2O.
点评 利用化学反应方程式和质量守恒定律来推断物质的化学式,应抓住反应前后原子的种类和数目不变.


科目:初中化学 来源: 题型:选择题
| A. | 应密封保存 | B. | 完全燃烧的反应属于分解反应 | ||
| C. | 可用作燃料 | D. | 肼的相对分子质量是32 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 实验现象 | 实验结论 |
| 维生素C可以降低泡菜中NaNO2的含量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将工厂污水直接排入河道,降低工厂成产成本 | |
| B. | 通过加高烟囱排放工业废气,较少地面空气污染 | |
| C. | 提倡步行、骑公共自行车等“低碳”出行方式 | |
| D. | 施用大量的化肥和农药以提高农作物产量 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
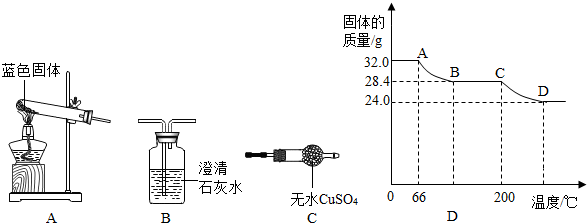
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com