
史上最贵”的实验:
步骤Ⅰ.让金刚石在充足的氧气中燃烧,收集生成的 气体;
气体;
步骤Ⅱ.让足量镁条在步骤Ⅰ生成的气体中燃烧,生成黑色的炭粉和白色的固体氧化物。
(1)步骤Ⅱ中发生反应的化学方程式:___________________,基本反应类型是_________。
(2)若金刚石质量为m1,按上述步骤反应且转化完全,生成的炭粉质量为m2,则m1____m2(填“<”、“=”、“>”),理由为___________________________________________。
科目:初中化学 来源: 题型:
逻辑推理是化学学习中常用的思维方法。下列推理正确的是:
A. 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
B. 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物
C. 单质中只含有一种元素,所以只含有一种元素的物质一定是单质
D. 在同一化合物中,金属元素显正价,所以非金属元素一定显负价
查看答案和解析>>
科目:初中化学 来源: 题型:
下列关于物质组成与分类的说法中正确的是( )
|
| A. | 含有氧元素的化合物叫做氧化物 |
|
| B. | 氢氧化钠的构成粒子是Na+和OH﹣ |
|
| C. | 原子核是由质子和电子构成的 |
|
| D. | NH3由一个氮元素和三个氢元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:
华雪同学想测定某Cu﹣Ag合金中两种金属的质量比.称取这种合金9.6g,加入足量AgNO3溶液充分反应后过滤,将所得固体洗涤、干燥后称量,质量为24.8g.
(1)发生反应的化学方程式为 .
(2)试计算该合金中铜与银的质量比.(请写出计算过程)
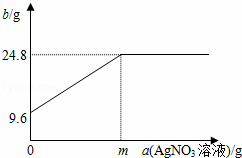
(3)华雪同学认为还可算出该AgNO3溶液中溶质的质量分数,于是进行了多次实验,记录了每次使用AgNO3溶液的质量a(AgNO3溶液)和充分反应后所得固体的质量b,并绘制了如图,则AgNO3溶液中溶质的质量分数是多少?(请写出计算过程,用含m的代数式表示)【出处.
查看答案和解析>>
科目:初中化学 来源: 题型:
新装修房室内存在甲醛(CH2O)、苯(C6H6)等有害物质。下列叙述正确的是
A.甲醛分子中含有水分子 B.甲醛中碳元素质量分数为40%
C.苯中碳元素与氢元素的质量比为1:1 D.甲醛和苯都属于无机化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
有关NaOH与CO2反应的探究
探究一:检验NaOH固体样品露置空气中一段时间后的成分
【查阅资料】Na2CO3溶液是碱性;KCl溶液、BaCl2溶液显中性、BaCO3难溶于水。
(1)检验样品是否变质。检验样品成分中是否含碳酸根的实验方法(操作、现象及结论):
___________________________________________________________________________。
(2)检验样品是否完全变质。实验操作:取样品加水溶解,先加过量的_________(填编号,下同),再滴加________。
A.盐酸 B.KCl溶液 C.BaCl2溶液 D.Ba(OH)2溶液 E.酚酞试液
 探究二:用NaOH溶液测定空气中酸性气体(CO2、SO2)的体积分数
探究二:用NaOH溶液测定空气中酸性气体(CO2、SO2)的体积分数
【实验装置】如图8所示,向细玻璃管内注入少量水,形成一段水柱;经检查该装置气密性良好。已知细玻璃管单位长度的容积为0.1mL·cm—1。水柱的质量忽略不计。
【操作步骤】保持外界条件不变,完成以下操作:
① 将40mL浓NaOH溶液迅速倒入烧瓶内,立即塞紧橡皮塞,并在细玻璃管 上标记水柱底部的位置
上标记水柱底部的位置
② 观察并测量得出水柱缓慢向下移动的距离为2.0cm;
③ 实验结束后,根据①中的标记,测得该标记以下细玻璃管及烧瓶的总容积为340mL。
(3)检查图8装置气密性的操作方法:___________________________
___ ________________________________________________。
________________________________________________。
(4)仅根据本次测量数据,该气体样品中酸性气体的体积分数为________(精确到0.00001)。
(5)在上述操作步骤②中,若装置温度略有升高,实验结果______(填“偏大”、“不变”或“偏小”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
钠及其化合物是中学化学学习和研究的重要内容。
 (1)右图是钠的原子结构示意图。下列说法不正确的是_______。
(1)右图是钠的原子结构示意图。下列说法不正确的是_______。
a. 钠属于金属元素 b. 钠原子的质子数为11
c. 钠离子的符号为Na+ d.钠在化学反应中易得到电子
(2)钠与水反应生成氢氧化钠和氢气,化学方程式为________;小苏打受热分解成碳酸钠、二氧化碳和水,化学方程式为________。
 (3)配制一瓶右图溶液需氯化钠_______g;配制50g 6%氯化钠溶液,若用量筒量取水时俯视读数(其他操作正确),则溶液的质量分数______6%(填“>”、“<”或“=”)。
(3)配制一瓶右图溶液需氯化钠_______g;配制50g 6%氯化钠溶液,若用量筒量取水时俯视读数(其他操作正确),则溶液的质量分数______6%(填“>”、“<”或“=”)。
(4)已知2Na2O2+2H2O =4NaOH+O2↑;2Na2O2+2CO2=2Na2CO3+O2 。实验室敞口放置的过氧化钠(Na2O2)已部分变质,取少量该固体样品于试管中,加足量水,可观察到什么现象?如何检验该水溶液中含有的氢氧化钠?(请简要写出实验步骤和现象)
(5)钛和钛合金性能优良,广泛用于航空、造船和化学工业中。工业上常用钠来制取钛,在高温时,钠与四氯化钛(TiCl4)反应生成氯化钠和钛。若用该方法制取2.4kg钛,理论上需要钠的质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
铝是生活中常见的金属。
(1)金属铝常用做导线是利用它的 性;
(2)金属铝表面常有一层致密的氧化膜,氧化膜主要成分是 (填名称或化学式);
(3)资料显示:铝与氢氧化钠和水反应生成偏铝酸钠(NaAlO2)和氢气;用56.25g 含杂质
4%的铝片(杂质对产生氢气的质量无影响)与足量的氢氧化钠和水充分反应,生成氢气的
质量为 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com