
| A. | 均一、稳定的液体不一定是溶液 | |
| B. | 用X射线检查肠胃病时,让病人服用的钡餐是硫酸钡的乳浊液 | |
| C. | 自行车链条涂油既防锈又能润滑减轻磨损 | |
| D. | 农业上,可以用氯化钠溶液来选种 |
科目:初中化学 来源: 题型:选择题
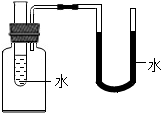 如图所示,向小试管中分别加入下列一定量的物质,右侧U型管中的液面左侧上升、右侧下降,该物质是( )
如图所示,向小试管中分别加入下列一定量的物质,右侧U型管中的液面左侧上升、右侧下降,该物质是( )| A. | 硝酸铵 | B. | 氢氧化钠固体 | C. | 蔗糖固体 | D. | 氧化钙固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳是常用的灭火剂,金属镁着火却不能用二氧化碳扑灭 | |
| B. | 在一般情况下,二氧化碳不能支持其它物质的燃烧,却可以支持镁的燃烧 | |
| C. | 反应前后,Mg、C、O三种元素的化合价都没有改变 | |
| D. | 该反应为放热反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 逐步淘汰高耗水生产工艺 | B. | 农田采用大水漫灌的方式 | ||
| C. | 减少农药、化肥的使用 | D. | 加强对水资源的监测 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方法 | 实验现象 | 结论 |
取两瓶未知气体,分别 通入澄清石灰水 | 第一个瓶子中无明显变化 第二个瓶子中产生白色浑浊 | 第一个瓶子中的气体为氧气 第二个瓶子中的气体为二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 野火烧不尽,春风吹又生 | B. | 粉身碎骨浑不怕,要留清白在人间 | ||
| C. | 只要功夫深,铁杵磨成针 | D. | 爆竹声中一岁除,春风送暖入屠苏 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
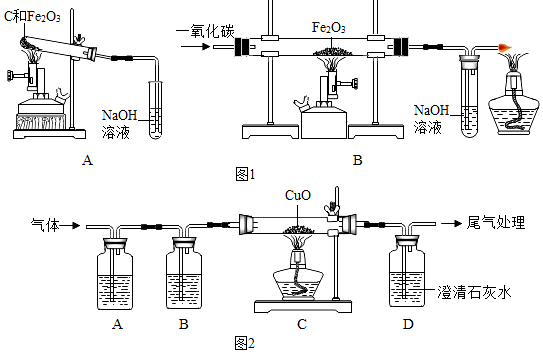

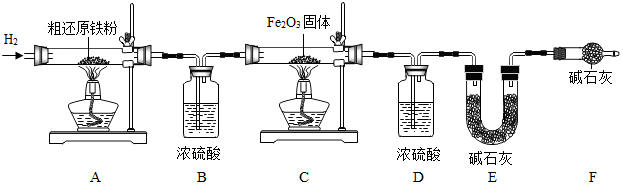
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com