
【题目】请回答下列问题:
(1)从 Na,O,C,H,Ca五种元素中选择适当元素,写出符合下列要求的各物质的化学式:
葡萄糖的化学式_______;具有还原性的有毒气体______;常见制氧物质_______改良酸性土壤的碱________;小苏打_______;2个碳酸根离子_________
(2)现有铁、氧化铜、稀盐酸、氢氧化钠溶液、硫酸铜溶液五种物质,两两混合能发生的反应有______个。写出其中一个反应的方程式_________
(3)已知浓硝酸(HNO3)见光会发生分解反应,生成红棕色的NO2气体和一种常见液体以及能供给呼吸的气体,写出该反应的化学方程式___________;
(4)某CaCl2样品中,可能含有 KNO3、CuCl2、MgCl2、NaCl 和 Na2CO3中的某些物质,取该样品m克溶于适量水中,得到澄清的无色溶液,然后向其中加入足量AgNO3溶液,得到n克白色沉淀,则该样品组成中,肯定没有的是:_______。
(5)粗盐中含有泥沙、CaCl2、MgCl2、Na2SO4杂质,在粗盐提纯过程中,通常先将粗盐溶于水,再依次滴加过量的______(填序号),(可选用的试剂:①Na2CO3溶液,②BaCl2溶液,③NaOH 溶液,)待充分反应后过滤,再向滤液中滴加适量的______,然后蒸发溶剂得到精盐。
(6)下图是甲、乙、丙三种固体物质的溶解度曲线图.

①要从甲的饱和溶液中析出晶体甲,可采用的方法是_____(只填一种).
②取 t1℃时甲、乙、丙的饱和溶液分别升温至 t2℃,三者所得溶液中溶质的质量分数大小关系为_______(用“>”、“<”或“=”表示)
③分别将t2℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是________。
【答案】C6H12O6 :CO; H2O2; Ca(OH)2; NaHCO3; 2CO32-; 5 Fe+2HCl==FeCl2+H2↑ 4HNO3![]() NO2+2H2O+O2↑ CuCl2、Na2CO3 ②①③ 稀盐酸 降温结晶法 乙>甲>丙 乙>甲>丙
NO2+2H2O+O2↑ CuCl2、Na2CO3 ②①③ 稀盐酸 降温结晶法 乙>甲>丙 乙>甲>丙
【解析】
(1)葡萄糖的化学式为:C6H12O6,故填:C6H12O6;
具有还原性的有毒气体:CO,故填:CO;
常见制氧物质:H2O2,故填:H2O2;
改良酸性土壤的碱:Ca(OH)2,故填:Ca(OH)2;
小苏打主要成分:NaHCO3,故填:NaHCO3;
碳酸根离子:CO32-,故填:2CO32-;
(2)现有铁、氧化铜、稀盐酸、氢氧化钠溶液、硫酸铜溶液五种物质,两两混合能发生的反应有:铁+稀盐酸、铁+硫酸铜溶液、氧化铜+稀盐酸、稀盐酸+氢氧化钠溶液、氢氧化钠溶液+硫酸铜溶液,共5个,故填:5;其中一个反应的方程式:Fe+2HCl==FeCl2+H2↑,故填:Fe+2HCl==FeCl2+H2↑。
(3)已知浓硝酸(HNO3)见光会发生分解反应的化学方程式为:4HNO3![]() 4NO2+2H2O+O2↑,故填:4HNO3
4NO2+2H2O+O2↑,故填:4HNO3![]() NO2+2H2O+O2↑。
NO2+2H2O+O2↑。
(4)CaCl2样品溶于适量水中,得到澄清的无色溶液可知样品中无CuCl2(溶于水有色)和Na2CO3(与CaCl2不共存)。故填:CuCl2、Na2CO3。
(5)除去CaCl2、MgCl2、Na2SO4分别加入①Na2CO3溶液,③NaOH 溶液,②BaCl2溶液,但加入碳酸钠的作用还有除去过量的BaCl2,故②要在①前,故填:②①③。过量的氢氧化钠和碳酸钠可以用稀盐酸除去,故填:稀盐酸。
(6)①甲物质的溶解度随温度升高而增大,且变化幅度较大,故可用降温结晶法从甲的饱和溶液中析出晶体甲,故填:降温结晶法;
②t1℃时甲、乙、丙的饱和溶液分别升温至 t2℃,甲、乙溶液为不饱和溶液,溶质质量分数乙>甲,丙溶液为过饱和溶液,溶质质量分数最小,三者所得溶液中溶质的质量分数大小关系为乙>甲>丙,故填:乙>甲>丙。
③分别将t2℃时甲、乙、丙的饱和溶液降温至t1℃,甲、乙溶液为饱和溶液,溶质质量分数乙>甲,丙溶液为不饱和溶液,溶质质量分数小于甲,故填:乙>甲>丙。


科目:初中化学 来源: 题型:
【题目】中国首位诺贝尔医学奖获得者屠呦呦继发现青蒿素后又发明了双氢青蒿素.图示是双氢青蒿素片的部分说明,请回答:

(1)双氢青蒿素中C:H:O的原子个数比为_____;
(2)双氢青蒿素分子的相对分子质量为_____;
(3)双氢青蒿素中H:O元素的质量比为_____;
(4)双氢青蒿素中所含碳元素的质量分数为_____;
(5)3片双氢青蒿素所含碳元素的质量为_____mg。(计算结果精确到0.1mg)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像能正确反应其对应的实验操作的是( )
A. 一定温度下,向接近饱和的硝酸钾溶液中不断加入硝酸钾固体
一定温度下,向接近饱和的硝酸钾溶液中不断加入硝酸钾固体
B.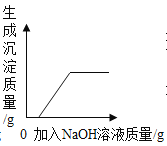 向硫酸和硫酸铜混合溶液中滴加过量的氢氧化钠溶液
向硫酸和硫酸铜混合溶液中滴加过量的氢氧化钠溶液
C.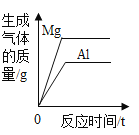 将等质量的镁粉和铝粉分别与足量等浓度的稀硫酸反应
将等质量的镁粉和铝粉分别与足量等浓度的稀硫酸反应
D.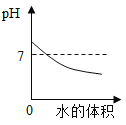 服用胃舒平[主要成分Al(OH)3]治疗胃酸过多,胃液pH的变化
服用胃舒平[主要成分Al(OH)3]治疗胃酸过多,胃液pH的变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图表示的是地壳中各元素的质量分数。请根据图示回答问题:

(1)图中表示出的金属元素有_________种;
(2)地壳中含量最多的金属元素与含量最多的非金属元素形成的化合物是_______(填化学式);
(3)硅常用做半导体,是集成电路的主要材料,硅是由________(填“原子”、“分子”或离子)构成的;
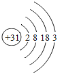
(4)合成材料纳米氮化镓我国十大科技成果之一。已知镓(Ga)元素的原子结构示意图如图,则氮化镓的化学式是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列装置回答问题:
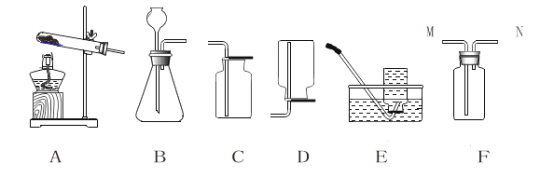
(1)实验室用高锰酸钾制氧气,应选择的发生装置是_________(填字母),组装好装置后首先应进行的操作是________________,若用E装置来收集氧气,收集氧气的适宜时机是 __________________,收集过程中发现水槽中的水变为紫红色,其原因是 ________________,待氧气收集完毕后,测得氧气的纯度明显偏低,其原因可能是_____________(填字母)。
a高锰酸钾中混入了二氧化锰 b收集前,集气瓶中未注满水
c收集后,集气瓶中仍有少量水 d加热前就将导管伸入集气瓶
(2)实验室选用 B 装置制取氧气,则从长颈漏斗中加入的药品是___________(填名称),该反应的符号表达式为_______________,若将长颈漏斗换成注射器,这样改进的优点是_______________。
(3)比较实验室用加热高锰酸钾与分解过氧化氢溶液两种方法制取氧气,使用分解过氧化氢溶液制氧气的优点是______________(写一条即可)。
(4)氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水。实验室常用加热氯化铵和氢氧化钙的固体混合物制取氨气,应选择的发生装置是____________,如果选用 F 装置收集 NH3,则 NH3 应从导管________端通入。
(5)已知实验室制取一瓶NO气体时选用 E 作为收集装置,而不能选用 C 或 D 装置来收集,由此可以推断NO气体可能具有的性质是___________(填序号)。
①能溶于水 ②密度比空气大 ③难溶于水 ④能和空气中某种气体发生反应 ⑤与水发生反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是研究物质的组成、结构、性质以及变化规律的科学,研究元素知识是学好化学的基础。下表包含部分元素的相关信息,完成以下填空:
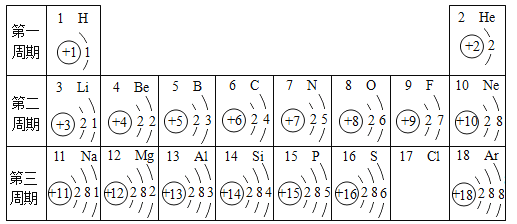
(1)1869年,科学家__________发现了元素周期律并绘制了元素周期表。
(2)请画出17号元素原子结构示意图___________, 9号元素在化学反应中比较容易________(填“得到”或“失去”)电子变成______(填“阴”或“阳”)离子。13号元素在化学反应中比较容易________(填“得到”或“失去”)电子后的粒子结构示意图___________。
(3)上表中12号元素与地壳中含量最多的元素组成的化合物是________(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质溶解度曲线,a与c溶解度曲线相交于P点。据图回答:
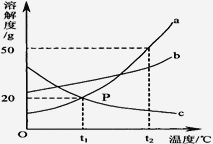
(1)t2℃时a物质的溶解度是____________。
(2)t2℃时30g a物质加到50g水中不断搅拌形成溶液的质量_____。
(3)t1℃时a、b、c三种物质的溶解度按由小到大的顺序排列是_____________(填写物质序号)。
(4)将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大到小关系是_____________。
(5)当a物质中混有少量b物质时,可采用___________方法提纯得到a物质。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学用语表达正确的是( )
A. 2Na:“2”表示两个钠元素
B. 氯化银的化学式为AgCl2
C. ![]() :“+2”表示一个镁离子带两个单位的正电荷
:“+2”表示一个镁离子带两个单位的正电荷
D. SO2:“2”表示一个二氧化硫分子中含有两个氧原子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用适当的数字和化学符号填空:
(1)氦气中氦元素的化合价______________;
(2)硝酸铵中的阴离子______________;
(3)与氖原子核外电子排布相同的阳离子_____________;(写一种即可)
(4)人体内含量最多的氧化物______________;
(5)地壳中含量最多的金属元素______________;
(6)由3个氧原子构成的分子______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com