
| 实验操作 | 实验现象 | 实验结论 |
| 取11.6g纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式 Na2CO3+CaCl2═CaCO3↓+2NaCl |
分析 (1)根据滴加的CaCl2溶液要过量的原因与碳酸钠充分反应进行解答;
(2)根据碳酸钙的质量计算碳酸钠的质量,进一步计算碳酸钠的质量分数;
(3)根据空气中含有二氧化碳进行解答;
(4)根据盐酸和碳酸钠反应生成氯化钠、水和二氧化碳进行书写化学方程式;
(5)根据质量守恒定律可知装置C中反应前后的质量差就是产生CO2的质量进行解答.
解答 解:
(1)滴加的CaCl2溶液要过量的原因与碳酸钠充分反应;故填:产生白色沉淀与碳酸钠充分反应;
(2)设Na2CO3的质量为x;
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10g
$\frac{106}{x}=\frac{100}{10g}$
x=10.6g
Na2CO3的质量分数为$\frac{10.6g}{11.6g}×100%$=91.4%
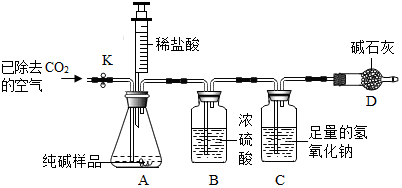
(3)空气中含有二氧化碳,所以打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳,再接上装置C和D;
(4)盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,故其反应的化学方程式为:
Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(5)由质量守恒定律可知装置C中反应前后的质量差就是产生CO2的质量,装置D的作用是防止空气中的二氧化碳和水蒸气进入装置C,所以若没有装置D,将会使测定结果偏大.
故答案为:
(1)产生白色沉淀与碳酸钠充分反应;
(2)91.4%;
(3)二氧化碳;
(4)Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(5)C;偏大.
点评 本题将计算和实验有机地结合起来进行考查,通过认真审题,结合题干中已给出一系列的提示,根据提出的问题,发现有用的信息,充分发挥联想,与已有的知识建立联系,然后进行类比推导,从而达到解决问题的目的.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 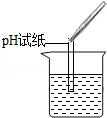 |  |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 产生白色沉淀 | |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 |
| 取少量滤渣于试管中,加入足量 稀硝酸 | 固体部分溶解,产生气泡 |

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 往水样中滴加几滴肥皂水,振荡,有大量泡沫出现的是硬水 | |
| B. | 电解水能生成H2和O2,二者体积比为1:2 | |
| C. | 用加热蒸发是否留有固体的方法可区分蒸馏水和食盐水 | |
| D. | 为防止水体污染,禁止使用化肥和农药 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com