
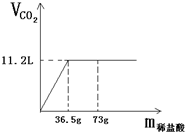
 现有80g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的体积与加入的稀盐酸的质量关系如图所示.试回答:
现有80g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的体积与加入的稀盐酸的质量关系如图所示.试回答:分析 (1)根据图象中二氧化碳的体积可求出二氧化碳的质量.质量=密度×体积;
(2)根据二氧化碳的质量可求出碳酸钙的质量,最后根据$\frac{碳酸钙}{石灰石的质量}$×100%可求出石灰石样品中碳酸钙的质量分数.
解答 解:(1)二氧化碳的质量=1.96g/L×11.2L≈22g
(2)设碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 22g
$\frac{100}{x}=\frac{44}{22g}$
x=50g
该石灰石样品中碳酸钙的质量分数=$\frac{50g}{80g}$×100%=62.5%
答:(1)22;
(2)石灰石样品中碳酸钙的质量分数为62.5%.
点评 求反应后所得溶液的质量的计算是初中化学计算的一个重点内容,其方法一般是:所加入的所有物质的质量总和-生成气体的质量-生成沉淀的质量.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
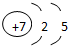 ,氮原子的最外层上的电子数为:5.
,氮原子的最外层上的电子数为:5.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 2010年8月26日蛟龙号深海载人潜水器成功下水,到达最大深度7062米,创造了世界同类作业型潜水器的最大下潜深度纪录.“蛟龙号”依靠充油银锌蓄电池可在水下作业9小时,“蛟龙”号“体积较小,没有潜艇那样的艇员生活设施,每次深海作业结束后,都会被回收到母船上补充能量和空气,而不是在海中独立行驶.请填写下列空白:
2010年8月26日蛟龙号深海载人潜水器成功下水,到达最大深度7062米,创造了世界同类作业型潜水器的最大下潜深度纪录.“蛟龙号”依靠充油银锌蓄电池可在水下作业9小时,“蛟龙”号“体积较小,没有潜艇那样的艇员生活设施,每次深海作业结束后,都会被回收到母船上补充能量和空气,而不是在海中独立行驶.请填写下列空白:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com