
【题目】硫酸是化工生产中重要的酸,其产量最大,用途最广,消耗量最多。历史上曾将硫酸的产量或消耗量作为一个国家化工生产发达程度的标志。
浓硫酸具有吸水性、脱水性和强氧化性。浓硫酸的腐蚀性主要是由它的脱水性和强氧化性引起的。稀硫酸有强酸性,稀硫酸的腐蚀性则主要是由酸性及水分蒸发后变浓而产生的。
硫酸的用途极广,常用于生产化肥、冶炼金属、农药、制药等。
工业制硫酸的流程为:FeS2![]() SO2
SO2 SO2
SO2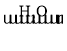 H2SO4
H2SO4
(1)综合分析以上材料,并结合已有知识,请回答:
①工业制H2SO4可能会引起的环境问题是_____。
②在实验室中不慎将浓硫酸沾到皮肤上的处理方法是_____。
A 立即用大量水冲洗,然后再涂上3%~5%的碳酸氢钠溶液。
B 立即用稀氢氧化钠溶液冲洗,然后再用水冲洗。
(2)某工厂化验室用9.8%的稀硫酸洗涤一定量化工产品中残留Ba(OH)2,当消耗稀硫酸100g时,沉淀不再产生,此时液体的pH=7(不考虑其它物质的影响),求化工产品中残留Ba(OH)2的质量。_____
科目:初中化学 来源: 题型:
【题目】(10分)某校化学兴趣小组就空气中氧气的含量进行了分组实验探究。
Ⅰ组:(1)Ⅰ组同学讨论后认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应而且生成物为固体。他们应该选择_________(填序号),为了充分消耗容器中的氧气,药品的用量应保证_______________________。
A.蜡烛 B.红磷 C.铁丝 D.木炭
(2)小组同学共同设计下图所示的两套装置,你认为合理的是______(填序号)。为了确保实验的成功,在装药品之前应该
____________________________________________。

(3)在讨论的基础上,他们分组进行了实验。
【数据分析】实验结束后,整理数据如下:(注:集气瓶容积为100 mL)
组别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入集气瓶中水的体积/mL | 20 | 21 | 19 | 20 | 22 | 19 |
(4)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的_________。
Ⅱ组:Ⅱ组同学发现Ⅰ组实验可能产生实验误差,对实验进行了改进,下图是Ⅱ组同学测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题。
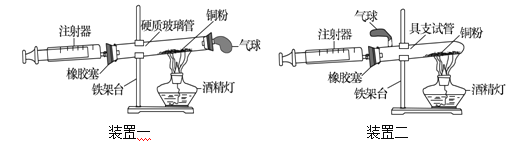
(1)根据下表提供的实验数据,完成下表
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
15mL | 15mL | 9mL |
(2)装置中气球的作用是 。
(3) 装置一和装置二中气球的位置不同, (填“装置一”或“装置二”)更合理,理由是 。
(4) 如何检查该装置的气密性? 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,某兴趣小组的同学为了探究酸碱盐之间能否发生反应做了以下几组实验。回答下列问题:
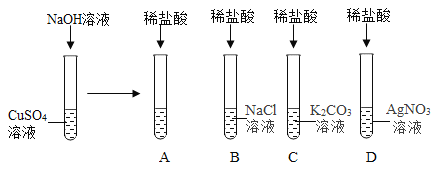
(1)向硫酸铜溶液中滴入氢氧化钠溶液,观察到的现象为_____,该反应的化学方程式为_____,继续滴加稀盐酸,通过稀盐酸与_____反应的现象证明了酸能与碱发生反应。
(2)B试管中无明显现象,不能发生复分解反应,理由是_____。
(3)观察到C试管中有_____生成,于是得出结论:稀盐酸能与碳酸钾发生反应。
(4)在D试管中有白色沉淀生成,于是得出结论:稀盐酸能与硝酸银发生反应。反应的化学方程式为_____。
(5)同学们对反应后C试管中溶液的溶质成分进行分析,得出以下结论
结论一:KCl
结论二:KCl、HCl;
结论三:_____。
某同学通过以下两种方法验证结论二是正确的。
实验操作 | 实验现象 | 实验结论 |
方法一:取C中溶液少许,加入足量的AgNO3溶液 | 产生白色沉淀 | 结论二正确 |
方法二:取C中溶液少许,加入适量的_____。 | 溶液颜色变红 |
(6)有些同学对方法一提出质疑,认为方法一不正确,理由是_____。当我们对反应后所得溶液的溶质成分进行猜想时,除了考虑生成物外,还要考虑_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁是几种常见的物质,分别由氢、碳、氧中的1~3种元素组成。
①甲是自然界中最硬的物质,其名称为____________。
②乙是最常用的溶剂,2摩尔乙中约含________个乙分子。
③丙是密度最小的气体,其摩尔质量为________。
④气体丁与氧气在点燃的条件下发生反应,其对应的微观示意图如下,请在方框中画出相应微粒的图示____________。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】周末的生活,丰富多彩。
晨练时,我们一家人去打了一场篮球。我知道涤纶运动衣、橡胶制的篮球和盛装用品的塑料筐都由_____材料制成。
上午,我在家看书。了解到1869年,俄国化学家门捷列夫(1834-1907)发现并编制了元素周期表,从此人们对化学的学习和研究有规律可循。在元素周期表与原子结构的关系中,原子序数=_____。
下午,爸爸妈妈带我去参观了制碱厂。制碱厂应用的是“侯氏联合制碱法”,其原理是我国化学工业的先驱侯德榜(1890-1974)创造的:X+NH3+CO2+H2O=NaHCO3↓+NH4Cl;2NaHCO3![]() Na2CO3+H2O+CO2↑。我知道了制碱厂的原料之一“X”是_____,产品“碱”是Na2CO3。
Na2CO3+H2O+CO2↑。我知道了制碱厂的原料之一“X”是_____,产品“碱”是Na2CO3。
晚上,电视节目中有这样一段情节:科考人员野外考察时要经过一小段沼泽地,为顺利通过,有人提议向沼泽地上铺一层生石灰,沼泽地将会变硬,人们能顺利通过,同时铺撒和通过时应小心“烫伤”。这是真的吗?我要继续看下去。我知道这一过程中的一个化学方程式是_____,并且能从化学角度说明“烫伤”的原因是_____。
学习了化学,我会用化学的眼光看生活,看世界!
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】几位同学根据下列各组实验装置图,设计和讨论了以下问题:
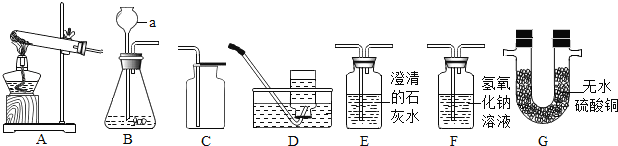
(1)
(ⅰ)实验仪器a的名称是_____.
(ⅱ)若用装置B、D制取氧气,反应的化学方程式为_____.
(ⅲ)用装置C收集的气体的密度比空气大,此外该气体还应具备的性质是_____.
(2)(ⅰ)铜锈的主要成分是Cu2(OH)2CO3,推测铜生锈除了与空气中的氧气和水有关外,还可能与空气中的_____有关.
(ⅱ)铜锈受热分解后的产物是氧化铜、二氧化碳和水,证明铜锈受热分解有二氧化碳和水生成的一整套实验装置的连接顺序为_____(填字母编号).
(ⅲ)U形管中的无水硫酸铜变为蓝色,证明产物中有水生成:证明产物中有二氧化碳生成的现象是_____.
(ⅳ)设计一个实验,验证铜锈受热分解后剩余的黑色固体是氧化铜(写出简要操作步骤,实验现象和结论)_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为甲、乙、丙三种固体物质的溶解度曲线图,请回答下列问题.
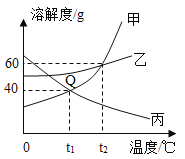
(1)Q点的含义是___________;
(2)若使接近饱和的丙溶液转变成饱和溶液,可采取的方法是___________(任写一种方法);
(3)甲中含少量乙时,可通过___________的方法提纯甲;
(4)t2℃时,将35g甲加入到50g水中,充分搅拌后,所形成溶液的质量为___________;
(5)将t2℃的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得三种溶液溶质质量分数关系正确的是___________(填选项字母).
A 甲=丙<乙 B 甲=乙>丙 C 乙>甲>丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】新型纳米材料MFe2Ox(3<X<4)中,M表示+2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,转化流程如下图所示:
![]()
已知MFe2Oy中Fe为+3价。下列说法中,不正确的是 ( )
A. SO2是大气污染物B. SO2不是该反应的催化剂
C. y的数值为4D. SO2发生了分解反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组用如图所示的装置来制取干燥的氧气,并测定H2O2溶液中溶质的质量分数。装置气密性良好,图I中的锥形瓶内盛有质量为m的H2O2溶液,燃烧匙内装有二氧化锰,燃烧匙可以上下移动,干燥管内装有足量碱石灰(CaO和NaOH的混合物)。下列说法正确的是( )
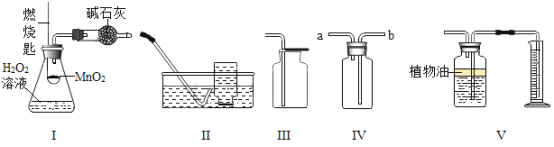
A.将装置I分别与装置Ⅱ、Ⅲ、Ⅳ、V连接,均能达到实验目的
B.称量装置I反应前及完全反应冷却后的质量,可计算出逸出的O2的质量
C.若用装置Ⅳ收集氧气,可将带火星的木条放置在b导管口处验满
D.若用装置 V 测量生成氧气的体积,集气瓶上方原有的空气会使测量结果偏大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com