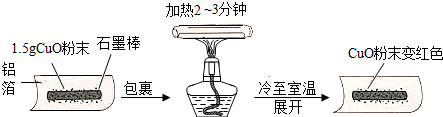
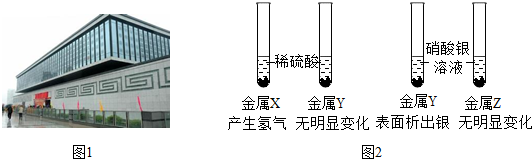
12.根据如图回答问题.

(1)实验室制取二氧化碳的化学方程式是CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑,选用的装置组合是CG(选填装置编号,下同).写出用该组合在实验室制取的另一种常见气体的化学方程式2H
2O
2$\frac{\underline{\;MnO_2\;}}{\;}$2H
2O+O
2↑.
某化学兴趣小组在老师指导下制取、干燥、收集氨气,并探究氨气的一些性质.
【查阅资料】
①氨气通常情况下是有刺激性气味的无色气体,密度比空气小,极易溶于水.
②氨水,主要成分NH
3•H
2O(一水合氨),氨气的水溶液,易挥发,具有部分碱的通性.NH
3•H
2O不稳定,受热易分解出氨气.
(2)将浓氨水滴加到固体烧碱上可以快速产生氨气,发生装置最好选用C.请写出固体烧碱在此过程中的作用:烧碱溶于水放出热量,促进氨水挥发.(任写一条)
(3)实验室通过直接加热浓氨水的方法也可以获得氨气,但混有大量水蒸气.现欲用此方法制取干燥的氨气,其装置组合是BDG.
如图为合成氨的模拟实验装置图(玻璃管中是铁粉和石棉绒组成的混合物).实验步骤:①检查装置气密性;②使锌粒和稀硫酸反应一段时间;③在Y型管盛有亚硝酸钠和氯化铵饱和溶液的一边加热(NH
4Cl+NaNO
2$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+2H
2O+N
2↑);④到产生氮气较快时,将酒精灯移至玻璃管下方加热.
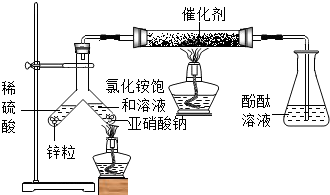
(4)反应开始前使锌粒和稀硫酸反应一段时间的目的是:排出装置内部的空气,防止可能发生的爆炸,同时生成尽可能多的氢气,提高氢气浓度从而提高氮气的转化率.
(5)当锥形瓶中出现酚酞溶液变红现象,表示有氨气生成.
(6)写出玻璃管中生成氨气的化学方程式:N
2+3H
2$\frac{\underline{催化剂}}{△}$2NH
3.

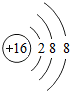
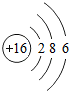 所表示的微粒属于同一种元素的是( )
所表示的微粒属于同一种元素的是( )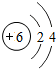
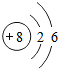
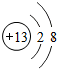
 53随堂测系列答案
53随堂测系列答案