
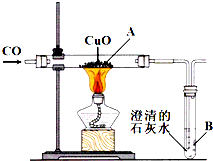
 如图为一氧化碳还原氧化铜的装置图:
如图为一氧化碳还原氧化铜的装置图: Cu+CO2 B处反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O
Cu+CO2 B处反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O Cu+CO2 CO2+Ca(OH)2=CaCO3↓+H2O
Cu+CO2 CO2+Ca(OH)2=CaCO3↓+H2O

科目:初中化学 来源: 题型:
| 实验内容 | 实验装置 | 过程与分析 | ||||||||
| 铁丝在纯氧中燃烧 |  |
如图所示,点燃火柴后立即连同铁丝快速深入集气瓶中下部(未接触水),但铁丝未燃烧,针对上述操作,请提出一条改进建议 待火柴快燃尽时,在将铁丝伸入集气瓶. 待火柴快燃尽时,在将铁丝伸入集气瓶. . | ||||||||
| 测定空气中O2的含量 |  |
①用聚光镜引燃白磷后夹紧弹簧夹. ②反应停止冷却至室温,打开弹簧夹,进入瓶内的水超过瓶容积的1/5. ③从操作角度分析,产生误差的原因可能是(写一点) 止水夹未夹紧 止水夹未夹紧 . | ||||||||
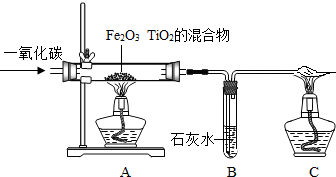
| 用草酸钠(Na2C2O4)分解产生的CO还原CuO(铁架台略) |  |
①实验开始,应先点燃A处酒精灯,过一会再点燃B处酒精灯,这样操作的目的是 点燃A处酒精灯,使草酸钠分解生成了一氧化碳,排净试管内的空气,防止爆炸 点燃A处酒精灯,使草酸钠分解生成了一氧化碳,排净试管内的空气,防止爆炸 .②B处玻璃管内的现象是 黑色粉末变成红色 黑色粉末变成红色 ,发生反应的化学方程式为CuO+CO
CuO+CO .
③该装置有待改进之处是 应添加尾气处理装置 应添加尾气处理装置 . |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 人类的生活离不开金属材料
人类的生活离不开金属材料
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验名称 | 实验设计 | 分析和回答的问题 | ||||||||
| a.电解水 |  |
(1)试管1中产生的气体为 氢气 氢气 (填名称);该实验说明水是由氢元素和氧元素 氢元素和氧元素 组成的. | ||||||||
| b.空气中 |  (燃烧匙中的药品为红磷) |
(2)实验中可观察到的现象是 红磷燃烧,集气瓶内充满白烟,打开弹簧夹后,水由烧杯流向集气瓶 红磷燃烧,集气瓶内充满白烟,打开弹簧夹后,水由烧杯流向集气瓶 ;某同学所得实验结果为集气瓶内的水上升至10%左右,其可能的原因是红磷量过少 红磷量过少 | ||||||||
| c.一氧化碳还原氧化铜 | 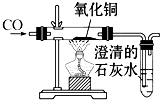 |
(3)写出该实验涉及的化学反应方程式: CO+CuO
CO+CuO .请你对如图所示的实验装置进行评价:
没有尾气处理装置. 没有尾气处理装置. |
查看答案和解析>>
科目:初中化学 来源: 题型:
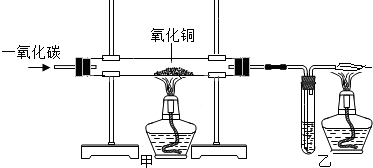
| 反应前 | 氧化铜完全反应后 | |
| Ⅰ组 | 洗气瓶和石灰水的质量为185g | 洗气瓶和瓶内物质的总质量为187g |
| Ⅱ组 | 玻璃管和氧化铜样品的质量为57.9g | 玻璃管和玻璃管内物质的质量为56.1g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com