
分析 (1)根据金属活动性顺序进行分析;
(2)根据碳酸氢铵在加热的条件下会分解生成氨气、水和二氧化碳,碳酸钙在高温的条件下生成氧化钙和二氧化碳进行分析;
(3)根据二氧化碳的密度比空气密度大进行分析;
(4)根据浓盐酸具有挥发性,浓度越大,挥发性越强进行分析.
解答 解:(1)锌的活动性排在氢的前面,铜的活动性排在氢的后面,所以金属活动性:锌>铜;
(2)碳酸氢铵在加热的条件下会分解生成氨气、水和二氧化碳,碳酸钙在高温的条件下生成氧化钙和二氧化碳,所以受热稳定性:碳酸钙>碳酸氢铵;
(3)二氧化碳的密度比空气密度大;
(4)浓盐酸具有挥发性,浓度越大,挥发性越强.
故答案为:(1)>;
(2)>;
(3)<;
(4)<.
点评 本题考查金属活动性顺序、物质的稳定性、气体的密度、浓盐酸的挥发性,要求我们对各个知识点都熟悉,并能进行正确比较.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | |

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 温度(℃) | 0 | 20 | 40 | 60 | 80 |
| 溶解度(g) | 13.3 | 31.6 | 63.9 | 110 | 169 |
| A. | KNO3的溶解度随温度的上升而变大 | |
| B. | 20℃时,100g饱和KNO3溶液中含有31.6gKNO3 | |
| C. | 将40℃的KNO3饱和溶液升温至60℃,该溶液变成不饱和溶液 | |
| D. | 将80℃的KNO3饱和溶液降温至20℃,有晶体析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
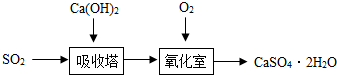 我国大气污染的主要来源是生产和生活使用化石燃料、燃煤等,SO2是主要大气污染物之一,用石灰浆吸收SO2转化为石膏是一种工业上烟气脱硫的方法如图:
我国大气污染的主要来源是生产和生活使用化石燃料、燃煤等,SO2是主要大气污染物之一,用石灰浆吸收SO2转化为石膏是一种工业上烟气脱硫的方法如图:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
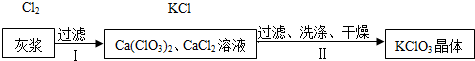
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 颜色发生变化 | B. | 发生了化学变化 | ||
| C. | 质量减少 | D. | 溶质质量分数变小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com