
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入的稀硫酸的质量/g | 5 | 5 | 5 | 5 |
| 烧杯中剩余固体的质量/g | 4.2 | 3.4 | 3.0 | 3.0 |
分析 向氧化铜和铜的混合物样品中加入稀硫酸,氧化铜与硫酸发生反应生成硫酸铜和水而铜不能与硫酸反应,因此随稀硫酸的加入固体粉末质量减少即由于氧化铜逐渐溶解于稀硫酸的结果.因此,由反应记录数据分析剩余固体质量可判断出混合物中铜的质量、氧化铜的质量,从而利用反应的化学方程式计算出硫酸铜的质量,进而求反应后所得溶液中硫酸铜的质量分数.
解答 解:(1)氧化铜中铜元素和氧元素的质量比为:64:16=4:1;
(2)硫酸分子中各原子的个数比H:S:O=2:1:4;
(3)由于氧化铜能与硫酸反应逐渐溶解而铜不能与硫酸反应,因此可判断第4次加入稀硫酸固体质量不再减少,此时固体全部为不能与硫酸反应的铜;即样品中铜的质量为3.0g;
(4)设生成硫酸铜的质量为x
H2SO4+CuO═CuSO4+H2O
80 160
5g-3g=2g x
$\frac{80}{160}=\frac{2g}{x}$
x=4g
第4次反应后所得溶液中硫酸铜的质量分数:$\frac{4g}{2g+20g}×100%$=18.2%.
答:第4次反应后所得溶液中硫酸铜的质量分数为18.2%.
点评 根据混合物中两物质的性质,分析反应中固体质量减少的原因,从而得到混合物组成成分的质量关系


科目:初中化学 来源: 题型:实验探究题


查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | NaOH溶液(Na2CO3) | 加入适量的Ca(OH)2溶液、过滤 |
| B | Fe(Cu) | 加足量稀硫酸后过滤 |
| C | CO(CO2) | 通过足量的NaOH溶液、干燥 |
| D | FeSO4溶液(H2SO4) | 加入足量Fe粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 实验操作 | 预期现象 | 结论 |
| 步骤1: 取少量原固体样品于试管中,逐渐加水并不断搅拌至烧杯内固体不再溶解 | 有白色固体 | 假设1成立 |
| 步骤2: 向步骤1反应后的白色固体中滴加足量稀稀HNO3溶液,并不断震荡 | 白色固体完全溶解,有气泡产生 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质).其中B是密度最小的气体,C为红色固体单质,请回答下列问题:
如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质).其中B是密度最小的气体,C为红色固体单质,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 木炭在氧气中燃烧,发出白光 | |
| B. | 打开盛有浓盐酸的试剂瓶,看到瓶口有大量白雾 | |
| C. | 把干燥的紫色石蕊小花放入盛满干燥的二氧化碳气体的集气瓶中,紫色小花变红 | |
| D. | 熟石灰与铵态氮肥研磨,产生刺激性气味的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 定时间 | 5:05 | 5:10 | 5:15 | 5:20 | 5:25 | 5:30 | 5:35 |
| pH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 | 4.85 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
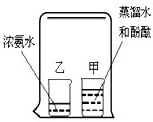 如图所示,在烧杯甲中装入蒸馏水,滴入几滴酚酞试剂,得到无色溶液.在烧杯乙中装入浓氨水.用一只大烧杯把甲、乙罩在一起.几分钟后,发现甲中的溶液变成红色.
如图所示,在烧杯甲中装入蒸馏水,滴入几滴酚酞试剂,得到无色溶液.在烧杯乙中装入浓氨水.用一只大烧杯把甲、乙罩在一起.几分钟后,发现甲中的溶液变成红色.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com