
【题目】某研究小组为验证铁、铜、锌、银的金属活动性顺序,设计如图所示三个实验(三种金属均已用砂纸打磨过,其形状和大小相同,稀盐酸的浓度和用量也相同)。
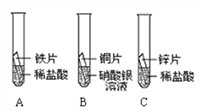
(1)一段时间后,观察到实验B的铜片表面有银白色固体附着,且溶液由无色变为______色,这说明铜比银的金属活动性______(选填“强”或“弱”),该反应的化学方程式为____________。
(2)甲同学认为通过实验A和C可比较锌和铁的金属活动性,他依据的实验现象是_________。
(3)乙、丙两位同学认为仅仅通过上述实验不足以得出四种金属的活动性顺序,因此在上述实验的基础上,两人分别选用不同的金属与不同的化合物溶液,各自补做了一个实验,装置均如下图所示,且都实现了探究目的。
![]()
乙同学的实验:X是金属________,丙同学的实验:Y是________溶液。
【答案】 蓝 强 Cu+2AgNO3===2Ag+Cu(NO3)2 根据反应的剧烈程度 Fe(或Cu) FeSO4溶液 (或CuSO4溶液)
【解析】(1)铜能与硝酸银反应生成硝酸铜和银,硝酸铜的溶液为蓝色,该反应的化学方程式为:Cu+2AgNO3===2Ag+Cu(NO3)2,说明铜比银的金属活动性强;(2)锌和铁都与盐酸反应,锌反应的速率比铁快,说明锌在铁的前面;(3)A能说明铁在氢的前面,B说明铜在银的前面,C说明锌在氢的前面,A、C说明锌在铁的前面,故通过A、B、C说明Zn>Fe>H,Cu>Ag,不能说明铁和铜的活动性,故可以通过金属与酸或金属与盐溶液的反应来证明铁和铜的活动性强弱。


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:初中化学 来源: 题型:
【题目】实验室常用双氧水和用二氧化锰作催化剂制取氧气。
【提出问题】
二氧化锰是催化剂,二氧化锰的用量对反应速率是否有影响?
【设计实验】
(1)实验装置如图所示。
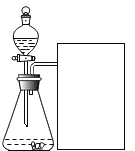
(2)实验记录:每次用30mL5%的过氧化氢溶液,采用不同量二氧化锰粉末做催化剂进行实验,测定相关数据记录于下表中:

【分析】
(1)写出该反应的文字表达式__________________________________________。
(2)上述实验应该测定的“待测数据(mL)”可能是_________________________。本实验中,测定“待测数据”的装置(图中方框内)是______(填序号)。
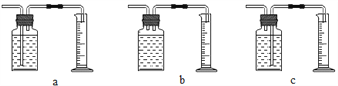
(3)3次实验“每次用30 mL 5%的过氧化氢溶液”的目的是_________________。
(4)若第Ⅱ次实验比第Ⅲ次实验的“待测数据”更________(填“大”或“小”),说明催化剂的用量越多,反应越快。二氧化锰可作为该反应的催化剂的依据是:加快该反应的反应速率,反应前后质量和_______________不改变。
(5)过氧化氢加热到80℃才有较多氧气生成,加入二氧化锰作为催化剂立即生成氧气。采用等量过氧化氢溶液,(虚线表示加热分解制取氧气的曲线,实线表示利用催化剂制取氧气的曲线),放出氧气的质量与反应时间的关系正确的是___________。
A.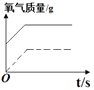 B.
B.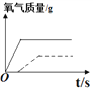 C.
C.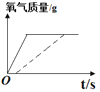 D.
D.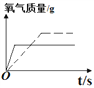
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据题意回答问题:
(1)A~F是初中化学中的常见物质,如图所示是它们之间的转化关系,图中部分反应物或生成物未全部标出。已知:A是天然气的主要成分,B在常温下为液态,F是黑色粉末。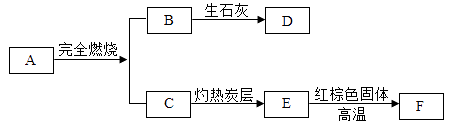
① A物质的化学式为;
② B→D是反应(填“放热”或“吸热”);
③ 在C→E的反应中,C物质发生(填“氧化反应”或“还原反应”);
④ 写出E→F反应的化学方程式:。
(2)设计对比实验,控制变量是学习化学的重要方法,下列对比实验不能达到目的的是。
编号 | A | B |
实验设计 |
|
|
实验目的 | 探究同种物质在不同溶剂中的溶解性 | 探究MnO2对过氧化氢分解的影响 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019世界环境日我国的主题是“蓝天保卫战,我是行动者”,下列做法符合这一主题的是
A.作物秸秆露天焚烧B.多使用一次性用品
C.禁止燃放烟花爆竹D.厨余垃圾焚烧处理
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com