
| A. | 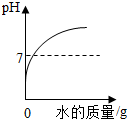 向一定量稀盐酸中加水稀释 | |
| B. | 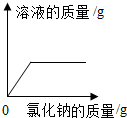 一定温度下,向不饱和食盐水中加入氯化钠 | |
| C. |  加热一定量的高锰酸钾固体 | |
| D. | 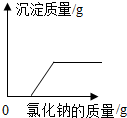 向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液 |
分析 A、稀盐酸呈酸性,其pH小于7,加水稀释,不会改变溶液的酸碱性,只会使溶液酸碱度增大到接近于7;
B、向不饱和食盐水中加入氯化钠,固体溶解,溶液质量增加,饱和后溶液质量不变,但注意开始不为零;
C、考虑高锰酸钾加热制取氧气会不断生产二氧化锰,锰元素的质量分数会不断增大,直到反应完成而不再变化;
D、硫酸铜和稀硫酸的混合液加入氢氧化钠,硫酸铜与氢氧化钠反应生成的氢氧化铜沉淀能与硫酸反应生成硫酸铜,故在硫酸铜和稀硫酸的混合液中硫酸首先与氢氧化钠反应,硫酸铜后与氢氧化钠反应解答
解答 解:
A、稀盐酸呈酸性,其pH小于7,加水稀释,不会改变溶液的酸碱性,只会使溶液酸碱度增大到接近于7,图象不符,故错误;
B、向不饱和食盐水中加入氯化钠,固体溶解,溶液质量增加,饱和后溶液质量不变,但注意开始不为零,图象不符,故错误;
C、高锰酸钾加热制取氧气会不断生产二氧化锰,锰元素的质量分数会不断增大,直到反应完成而不再变化,则图象错误,故B错误;
D、硫酸铜与氢氧化钠反应生成的氢氧化铜沉淀能与硫酸反应生成硫酸铜,故在硫酸铜和稀硫酸的混合液中氢氧化钠先和硫酸反应,后与氢氧化钠反应,也就是刚开始不能出现氢氧化铜沉淀,故D正确.
故选D.
点评 本题考查了了常见物质间的反应,完成此题,可以依据物质的性质以及反应的实质进行.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 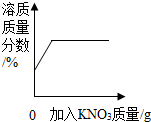 t℃时向不饱和KNO3溶液中加入KNO3固体 | |
| B. | 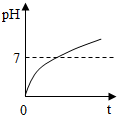 向盐酸中不断滴加氢氧化钾溶液 | |
| C. | 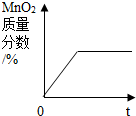 实验室用KClO3与MnO2共热制O2 | |
| D. | 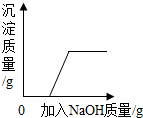 向盛有HNO3和Cu(NO3)2的溶液中加入NaOH溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
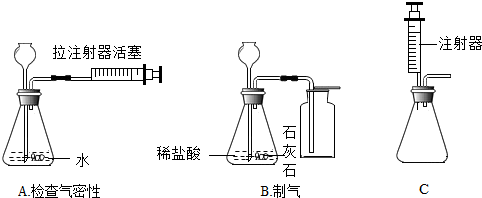
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
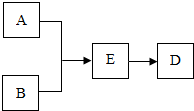 A、B、D、E是初中化学常见物质,分别由C、H、O、S、Ca、Fe等七种元素中的一种或几种组成,四种物质的转化关系如图所示,其中D在常温下为一种生命活动不可或缺的无色液体.其中“→”表示转化关系.
A、B、D、E是初中化学常见物质,分别由C、H、O、S、Ca、Fe等七种元素中的一种或几种组成,四种物质的转化关系如图所示,其中D在常温下为一种生命活动不可或缺的无色液体.其中“→”表示转化关系.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
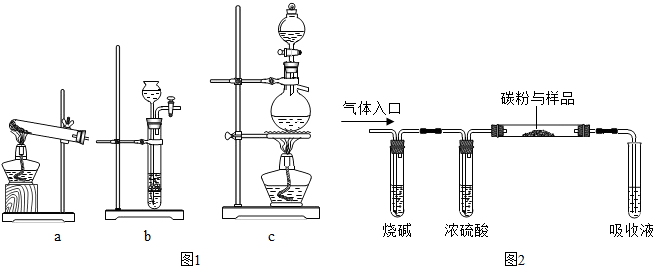
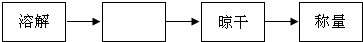
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com