
| A. | Na+ Ag+ S2- Cl- | |
| B. | Cu2+ Ca2+ OH- NO3- | |
| C. | Al3+ Fe3+ Cl- SO4 2- | |
| D. | K+ Mg2+ CO3 2- NO3- |
分析 pH为1的水溶液显酸性,水溶液中含有大量的H+.根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能大量共存.
解答 解:pH为1的水溶液显酸性,水溶液中含有大量的H+.
A、Ag+、Cl-结合生成不溶于酸的氯化银沉淀,不能大量共存,故选项错误.
B、OH-在溶液中与H+结合生成水,不能大量共存,故选项错误.
C、四种离子在溶液中不能结合生成沉淀、气体、水,能在酸性溶液中大量共存,故选项正确.
D、CO32-在溶液中与H+结合生成水和二氧化碳,不能大量共存,故选项错误.
故选:C.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水;还要注意是在酸性溶液中共存.


科目:初中化学 来源: 题型:选择题
| A. | 用NaCl溶液吸收 | B. | 用NaOH 溶液吸收 | ||
| C. | 用浓HCl溶液吸收 | D. | 用浓H2SO4溶液吸收 |
查看答案和解析>>
科目:初中化学 来源:江苏省2017届九年级中考模拟考试化学试卷 题型:信息分析题
矿山废水中含有大量的H2SO4和CuSO4,直接排放会影响水体酸碱性,并造成重金属污染。通过处理可以回收金属铜,并使废水pH和重金属含量达到排放标准。
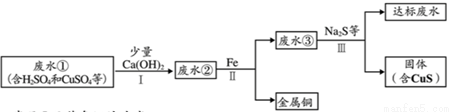
已知:步骤I无蓝色沉淀生成。
(1)步骤Ⅱ和步骤Ⅲ都需进行的操作是_______。
(2)步骤Ⅱ得到金属铜的反应的化学方程式为_______。
(3)加入Ca(OH)2可以降低铁屑的消耗量,原因是_______(请用文字并结合化学方程式解释)。
(4)步骤Ⅲ需加入Na2S才能使废水达到排放标准,由此推测废水③不达标的主要原因 是其中含有_______。
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 选项 | 物质 | 除杂试剂(足量) | 操作方法 |
| A | CO2(HCl) | 氢氧化钠溶液 | 气体通过盛有氢氧化钠溶液的洗气瓶 |
| B | NaCl(Na2CO3) | 盐酸 | 加入足量盐酸、蒸发、结晶 |
| C | MnO2(NaCl) | 水 | 加入足量水溶解、过滤、洗涤、干燥 |
| D | Cu(CuO) | 氧气 | 通入足量氧气并加热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注,常温下Ti不和非金属、强酸反应,红热时,却可与许多非金属单质反应,钛是航空、宇航、军工、电力等方面的必需原料.地壳中含钛矿石之一,称金红石(TiO2),目前大规模生产钛的方法是:首先将金红石、炭粉混合在高温条件下通入氯气制得TiCl4和一种可燃性气体,该步反应的化学方程式是TiO2+2C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO.第二是在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应,制得金属钛.此反应的化学方程式为2Mg+TiCl4$\frac{\underline{\;氩气\;}}{△}$2MgCl2+Ti.
钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注,常温下Ti不和非金属、强酸反应,红热时,却可与许多非金属单质反应,钛是航空、宇航、军工、电力等方面的必需原料.地壳中含钛矿石之一,称金红石(TiO2),目前大规模生产钛的方法是:首先将金红石、炭粉混合在高温条件下通入氯气制得TiCl4和一种可燃性气体,该步反应的化学方程式是TiO2+2C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO.第二是在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应,制得金属钛.此反应的化学方程式为2Mg+TiCl4$\frac{\underline{\;氩气\;}}{△}$2MgCl2+Ti.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源:江苏省2017届九年级中考模拟考试化学试卷 题型:选择题
下列变化中不涉及化学变化的是( )
A.金刚石刀切割玻璃 B.用粮食发酵酿酒
C.生石灰吸水变成粉末 D.铁矿石在高炉中炼铁
查看答案和解析>>
科目:初中化学 来源:江苏省无锡市长泾片2017届九年级下学期第二次模拟考试化学试卷 题型:简答题
氧化锌为白色粉末,无臭、无味,广泛应用于橡胶、涂料、陶瓷、化工、医药、玻璃和电子等行业,为了变废为宝,综合应用资源,经常从锌冶炼、锌制品加工企业回收的废渣(含有ZnO、FeO、Fe2O3、CuO等杂质)来制取氧化锌,其流程如下图所示:
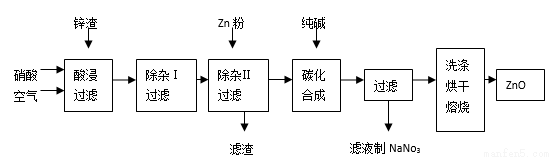
信息:1、3FeO+10HNO3==3Fe(NO3)3+NO+5H2O,NO有毒,能与氧气和水反应生成硝酸。 2、在“除杂Ⅰ”步骤中,只有铁离子能形成氢氧化铁沉淀。
回答下列问题
(1)在酸浸过程中,经常要保持酸过量,理由是________;通入空气的目的是:①起搅拌作用,使反应充分,②___________。通入空气反应的化学方程式为________________________________。
(2)在“除杂Ⅰ”步骤中,加入一种金属氧化物与过量的硝酸反应,使溶液pH升高为4左右,请结合本厂实际,可加入的物质是(______)
A、 ZnO B、 FeO C、Fe2O3 D、CuO
(3)为了使产品更加纯净,在“除杂Ⅱ”步骤中,滤渣的成分是_____________________。
(4)在“碳化合成”中,生成的产物之一为碱式碳酸锌[Zn2(OH)2CO3],还生成一种能使澄清石灰水变浑浊的气体氧化物。请写出碳化合成步骤的化学方程式__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | M | N | Q | P |
| 反应前质量(g) | 18 | 1 | 2 | 32 |
| 反应后质量(g) | X | 26 | 2 | 12 |
| A. | 该变化的基本反应类型是分解反应 | B. | 反应后物质X的值为l3 | ||
| C. | 反应中N、P的质量比为5:4 | D. | 物质Q可能是该反应的催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com