
分析 (1)根据pH的测定方法来分析;
(2)考虑氢气和氧气分别是由氢元素和氧元素组成的;
(3)考虑氧化钙与水反应,进行分析;
(4)考虑溶液所含金属离子不同;
(5)在鉴别这三种物质时,所选择的药品要出现三种不同的现象将这三种物质鉴别出来;三种固体溶于水会使溶液的温度发生改变:NaCl溶于水温度不变,NH4NO3溶于水温度降低,NaOH溶于水温度升高.
解答 解:(1)通常用pH试纸来测定溶液的酸碱度,故填:pH试纸;
(2)氢气和氧气分别是由氢元素和氧元素组成的,实验可以证明水是由氢、氧两种元素组成;
(3)将足量的CaO放入少量水中,氧化钙与水反应生成氢氧化钙,故水是反应物;
(4)因为FeCl3溶液呈黄色;FeCl2溶液呈浅绿色;故FeCl2和FeCl3两种物质的水溶液颜色不同,从微观的角度分析其原因是溶液所含金属离子不同;
(5)三种固体溶于水会使溶液的温度发生改变:NaCl溶于水温度不变,NH4NO3溶于水温度降低,NaOH溶于水温度升高,因此将固态的NaCl、NH4NO3、NaOH分别加入水中,温度升高的是氢氧化钠,温度降低的是硝酸铵,温度不变的是氯化钠.
故答案为:
(1)pH试纸.(2)氢气燃烧.(3)反应物,(4)溶液所含金属离子,(5)水温度升高.
点评 本题考查了酸碱度的测定以及物质的鉴别等,解题关键是熟悉要鉴别物质的性质,然后选择合适的试剂进行混合出现不同的现象即可.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
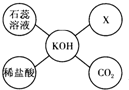 如图是氢氧化钾的化学性质知识网络图.
如图是氢氧化钾的化学性质知识网络图.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
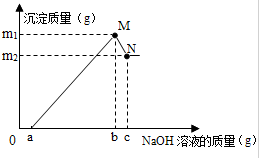 小明对废弃的易拉罐很有兴趣,为测定易拉罐中铝元素的质量分数,他剪取W克镁铝合金的易拉罐,先用过量稀硫酸溶解,然后再向溶液中滴加一定量的NaOH溶液得到Al(OH)3沉淀,继续滴加NaOH溶液时Al(OH)3被溶解[已知:Al(OH)3与NaOH反应成NaAlO2和H2O].而Mg(OH)2不溶于NaOH溶液,沉淀质量与滴加NaOH溶液质量关系如图所示
小明对废弃的易拉罐很有兴趣,为测定易拉罐中铝元素的质量分数,他剪取W克镁铝合金的易拉罐,先用过量稀硫酸溶解,然后再向溶液中滴加一定量的NaOH溶液得到Al(OH)3沉淀,继续滴加NaOH溶液时Al(OH)3被溶解[已知:Al(OH)3与NaOH反应成NaAlO2和H2O].而Mg(OH)2不溶于NaOH溶液,沉淀质量与滴加NaOH溶液质量关系如图所示查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 向A、B、C三只相同的玻璃杯中,分别注入等体积的蒸馏水,并在各玻璃杯外壁标明刻度,第一个玻璃杯用塑料保鲜膜包住杯口,第二个用报纸包住杯口,第三个玻璃杯敞口,如图所示放置一段时间后发现A杯中的水量几乎不变;而C杯中的水量减少较多;B杯中的水量减少比A杯多,比C杯少.根据以上信息回答问题:
向A、B、C三只相同的玻璃杯中,分别注入等体积的蒸馏水,并在各玻璃杯外壁标明刻度,第一个玻璃杯用塑料保鲜膜包住杯口,第二个用报纸包住杯口,第三个玻璃杯敞口,如图所示放置一段时间后发现A杯中的水量几乎不变;而C杯中的水量减少较多;B杯中的水量减少比A杯多,比C杯少.根据以上信息回答问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com