
| 实验步骤 | 实验现象 | 结论 |
①取少量废液于试管中,向其中滴加稀盐酸; ②继续加稀盐酸直到无气体冒出; ③③再滴加氯化钡溶液,观察现象 | 有气泡冒出 有白色沉淀产生 | 废液中有CO32- 废液中有SO42- 甲同学的假设成立 |
分析 [理论分析]:因为溶液显碱性,所以溶液中一定含有较多的OH-,根据复分解反应发生的条件即可分析出溶液中一定不存在H+;因为所有的硝酸盐、钠盐、钾盐均可溶于水,根据复分解反应发生的条件即可分析出答案;
[猜想与假设]:根据Ba2+可以与SO42-和CO32-反应,即可知丙不正确;
[实验验证]:根据SO42-和CO32-的检验方法去分析:CO32-可以与酸反应放出气体,SO42-与Ba2+反应生成白色沉淀.
解答 解:【理论分析】因为溶液显碱性,所以溶液中一定有OH-,根据复分解反应发生的条件,H+与OH-会发生反应,即两者不共存,所以溶液中一定不含H+;
因为所有的硝酸盐、钠盐、钾盐都可溶于水,根据复分解反应发生的条件,所以NO3-、K+、Na+这三种离子无论什么条件下都会存在.
故答案为:H+;Na+;
【猜想与假设】因为硫酸钡、碳酸钡是沉淀,所以Ba2+与SO42-和CO32-不能共存.
故答案为:丙;Ba2+与SO42-和CO32-不能共存;
【实验验证】我选择甲同学的假设,用下面的方法即可验证SO42-、CO32-.
取溶液少许,向溶液中加入稀盐酸,若有无色无味的气体冒出就可以说明溶液中有CO32-;继续加稀盐酸直到无气体冒出,然后向溶液中滴加氯化钡溶液,若有白色沉淀产生则证明溶液中也含SO42-.
故答案为:甲
| 实验步骤 | 现象 | 结论 |
| ①取少量废液于试管中,向其中滴加稀盐酸; ②继续加稀盐酸直到无气体冒出; ③③再滴加氯化钡溶液,观察现象 | 有气泡冒出 有白色沉淀产生 | 废液中有CO32- 废液中有SO42- 甲同学的假设成立 |
点评 检验混合溶液中的几种离子时,一定要注意排除其他离子的干扰,即确定了一种离子后,在验证下一种离子之前要除完全前一种离子,以免引起干扰.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
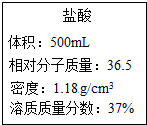 如图是实验室所用浓盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:
如图是实验室所用浓盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 2012年4月15日,央视《每周质量报告》报道:一些企业用皮革废料熬制工业明胶,在加工过程中添加重铬酸钾,在加热条件下重铬酸钾分解,反应的化学方程式为:4K2Cr2O7$\frac{\underline{\;\;△\;\;}}{\;}$4K2CrO4+2O3+3O2↑,工业明胶制造药用胶囊,导致胶囊重金属铬超标.铬是一种重金属元素,能对肝、肾等内脏器官和DNA造成损伤.在通常情况下,铬单质是银白色有金属光泽的固体,有较高的熔点,是最硬的金属;在加热时,能与浓硫酸反应生成硫酸铬(其中铬元素化合价为+3价),同时还生成一种大气污染物和一种常见的液体.
2012年4月15日,央视《每周质量报告》报道:一些企业用皮革废料熬制工业明胶,在加工过程中添加重铬酸钾,在加热条件下重铬酸钾分解,反应的化学方程式为:4K2Cr2O7$\frac{\underline{\;\;△\;\;}}{\;}$4K2CrO4+2O3+3O2↑,工业明胶制造药用胶囊,导致胶囊重金属铬超标.铬是一种重金属元素,能对肝、肾等内脏器官和DNA造成损伤.在通常情况下,铬单质是银白色有金属光泽的固体,有较高的熔点,是最硬的金属;在加热时,能与浓硫酸反应生成硫酸铬(其中铬元素化合价为+3价),同时还生成一种大气污染物和一种常见的液体.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 时间/S | 0 | 30 | 60 | 90 | 120 | 150 | 180 |
| 增加的质量/g | 0 | 30 | 50 | 60 | 66 | 66 | 66 |

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
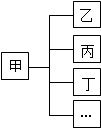 分类法是一种行之有效、简单易行的科学方法,人们在认识食物时可以采取多种分类方法.小军用如图所示形式对所学知识进行归纳,其中甲包括了乙、丙、丁…下列关系中,有错误的一组是( )
分类法是一种行之有效、简单易行的科学方法,人们在认识食物时可以采取多种分类方法.小军用如图所示形式对所学知识进行归纳,其中甲包括了乙、丙、丁…下列关系中,有错误的一组是( ) | 选项 | 甲 | 乙、丙 |
| A | 常见的干燥剂 | 浓硫酸、碱石灰、生石灰 |
| B | 常见的合金 | 不锈钢、焊锡、生铁 |
| C | 常见的碱 | 烧碱、纯碱、熟石灰 |
| D | 常见的营养物质 | 蛋白质、维生素、无机盐 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
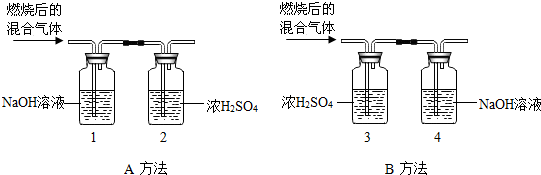
| 燃烧有机物的质量 | 实验方法 | 实验前后①-④装置质量 | ||
| 实验前 | 实验后 | |||
| 甲组 | 5.4g | A | ①150g | ①153.6g |
| ②150g | ②165.4g | |||
| 乙组 | 5.4g | B | ③150g | ③166.0g |
| ④150g | ④154.2g | |||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com