


分析 (1)根据氧化物是由两种元素组成的纯净物,其中一种是氧元素进行分析;
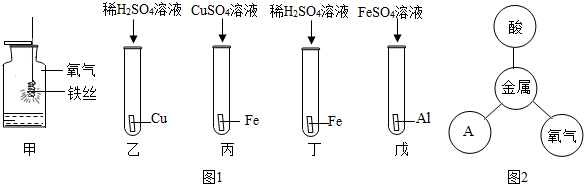
(2)①根据铁丝和氧气点燃生成四氧化三铁,铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
②根据题中的现象,确定金属的活动性顺序;
③根据活泼金属会与酸、氧气、盐反应进行分析;
(3)根据一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳进行分析;
(4)①根据物质的性质决定物质的用途;
②根据合金的性质比组成的纯金属的性质优良进行分析;
a、根据碱式碳酸铜和硫酸反应生成硫酸铜、水和二氧化碳进行分析;
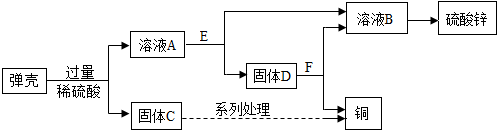
b、根据碱式碳酸铜能与硫酸反应生成硫酸铜、水和二氧化碳,硫酸铜能与锌反应生成硫酸锌和铜,溶液B是硫酸锌,固体D能与硫酸反应生成无色气体E,则D中除了含有铜,还含有锌,然后进行验证即可.
解答 解:(1)氧化物是由两种元素组成的纯净物,其中一种是氧元素,所以属于氧化物的是氧化铝,氧化铁,四氧化三铁,故选:ACD;
(2)①铁丝和氧气点燃生成四氧化三铁,反应现象为铁丝剧烈燃烧,火星四射,生成黑色固体,铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;
②只有乙中不反应,铁会与硫酸铜反应,所以铁比铜活泼,铁会与稀硫酸反应,所以铁比氢活泼,铝会与硫酸亚铁反应,所以铝比铁活泼,所以由强到弱的顺序是:Al、Fe、H、Cu;
③活泼金属会与酸、氧气、盐反应,所以图2中的A属于盐;
(3)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(4)①A、铁锅利用了铁的导热性,故A错误;
B、铜导线利用了铜的导电性,故B正确;
C、铝箔利用了铝的延展性,故C错误;
D、黄金饰品利用了金属的光泽,故D错误.
故选:B;
②合金的性质比组成的纯金属的性质优良,所以焊锡(主要含锡、铅)与其组成金属相比具有熔点低的特性;
a、碱式碳酸铜和硫酸反应生成硫酸铜、水和二氧化碳,化学方程式为:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑;
b、碱式碳酸铜与硫酸反应生成硫酸铜、水、二氧化碳,所以蓝色溶液B是硫酸铜溶液,E与硫酸铜溶液反应生成硫酸锌,所以E是锌,铁与硫酸铜反应生成了铜和硫酸锌,得到的固体D与硫酸反应后有气体生成,说明有锌剩余,锌与硫酸铜反应生成了铜,固体D中含有锌和铜.
故答案为:(1)ACD;
(2)①铁丝剧烈燃烧,火星四射,生成黑色固体,Fe+CuSO4=FeSO4+Cu;
②Al、Fe、H、Cu;
③盐;
(3)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(4)①B;
②熔点低;
a、Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑;
b、锌、铜.
点评 本题主要考查了金属有关的性质和金属活动性顺序的应用,难度不大,需要加强记忆.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 74.4% | B. | 80.0% | C. | 83.3% | D. | 92.6% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 地壳中含有的氧、硅、铝、铁.结合如图分析,关于这四种元素的说法正确的是(
地壳中含有的氧、硅、铝、铁.结合如图分析,关于这四种元素的说法正确的是(| A. | 氧原子核电荷数为8 | |
| B. | 硅元素属于金属元素 | |
| C. | 铝元素和氧元素形成化合物的化学式为Al3O2 | |
| D. | 铁的相对原子质量为55.85g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 试验次数 | 金属质量(g) | 金属氧化物质量(g) |
| 1 | 45.0 | 84.9 |
| 2 | 45.0 | 85.1 |
| 3 | 45.0 | 85.0 |
| 平均值 | 45.0 | m |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用肥皂水区分硬水和软水 | |
| B. | 用尝味道的方法区分厨房橱柜中调味品食盐和蔗糖 | |
| C. | 用灼烧的方法鉴别羊毛线和棉线 | |
| D. | 用白醋区分苏打和小苏打 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com