
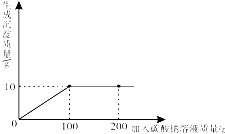
 小亮同学在某化工厂进行社会实践,技术员与小亮一起分析由氯化钙和氯化钠组成的产品中氯化钠的含量.现取14.4g固体样品,全部溶于95.6g水中,向所得的混合溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如图所示的曲线关系.试求:(本题计算结果保留一位小数)
小亮同学在某化工厂进行社会实践,技术员与小亮一起分析由氯化钙和氯化钠组成的产品中氯化钠的含量.现取14.4g固体样品,全部溶于95.6g水中,向所得的混合溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如图所示的曲线关系.试求:(本题计算结果保留一位小数)| 111 |
| x |
| 100 |
| 10g |
| 117 |
| y |
| 3.3g+11.7g |
| 14.4g+95.6g+100g-10g |


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、HCl、NaOH、NaCl |
| B、KNO3、NaCl、FeCl3 |
| C、NaOH、Na2CO3、NaCl |
| D、(NH4)2SO4、Ca(OH)2、NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com