
 如图是测定空气中氧气含量的实验装置,请根据实验回答问题
如图是测定空气中氧气含量的实验装置,请根据实验回答问题 的氧气完全消耗,气体减少了
的氧气完全消耗,气体减少了 ,因此可观察到钟罩内水面上升;红磷燃烧的化学方程式为4P+50
,因此可观察到钟罩内水面上升;红磷燃烧的化学方程式为4P+50 2P2O5;
2P2O5; 而不会继续上升,可说明剩余的氮气既不溶于水又不能与水发生反应;
而不会继续上升,可说明剩余的氮气既不溶于水又不能与水发生反应; ;4P+50
;4P+50 2P2O5;
2P2O5;

科目:初中化学 来源: 题型:
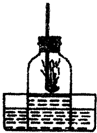 (2002?山东)如图是测定空气中氧气的体积分数的装置.将一钟罩放入盛水的水槽中,点燃燃烧匙里的药品,立即插入钟罩内,同时塞紧橡皮塞,反应结束后钟罩内水面上升了1/5体积.现有:①硫粉②红磷③木炭粉,燃烧匙中的药品最好选用( )
(2002?山东)如图是测定空气中氧气的体积分数的装置.将一钟罩放入盛水的水槽中,点燃燃烧匙里的药品,立即插入钟罩内,同时塞紧橡皮塞,反应结束后钟罩内水面上升了1/5体积.现有:①硫粉②红磷③木炭粉,燃烧匙中的药品最好选用( )查看答案和解析>>
科目:初中化学 来源: 题型:
 如图是测定空气中氧气体积分数的实验装置.
如图是测定空气中氧气体积分数的实验装置.
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
 如图是测定空气中氧气的含量的实验:(友情提示:本实验采用灼烧铜丝的方法)
如图是测定空气中氧气的含量的实验:(友情提示:本实验采用灼烧铜丝的方法)| 1 |
| 5 |
| 1 |
| 5 |
查看答案和解析>>
科目:初中化学 来源: 题型:
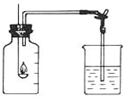 如图是测定空气中氧气含量的装置图:
如图是测定空气中氧气含量的装置图:| 1 |
| 5 |
| 1 |
| 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com