
菱铁矿(主要成分是FeCO3)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示
已知:①FeCO3+H2SO4=FeSO4+CO2↑+H2O ②菱铁矿中杂质不参加反应,且难溶于水.
请计算:
(1)20.0g菱铁矿中FeCO3的质量为 g
(2)列式计算所用稀硫酸的溶质质量分数(结果准确到0.1%)

考点:
根据化学反应方程式的计算;有关溶质质量分数的简单计算.
专题:
综合计算(图像型、表格型、情景型计算题).
分析:
剩余固体的质量即为杂质的质量,根据杂质的质量可以计算FeCO3的质量;
根据FeCO3的质量可以计算反应的硫酸的质量,进一步可以计算所用稀硫酸的溶质质量分数.
解答:
解:(1)20.0g菱铁矿中FeCO3的质量为:20.0g﹣8.4g=11.6g,
故填:11.6.
(2)设硫酸的质量为x,
FeCO3+H2SO4=FeSO4+CO2↑+H2O,
116 98
11.6g x
 =
= ,
,
x=9.8g,
所用稀硫酸的溶质质量分数为: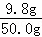 ×100%=19.6%,
×100%=19.6%,
答:所用稀硫酸的溶质质量分数为19.6%.
点评:
本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


科目:初中化学 来源: 题型:
如图表示某化学反应的微观过程,下列有关说法正确的是( )

|
| A. | 该反应属于化合反应 |
|
| B. | 反应物甲的质量等于生成物丁的质量 |
|
| C. | 甲和丙均为有机物 |
|
| D. | 甲的化学式为C2H2 |
查看答案和解析>>
科目:初中化学 来源: 题型:
区分下列物质选用的试剂或方法不能达到目的是( )
A.用氯化钡溶液区分稀盐酸和稀硫酸
B.用灼烧法区分棉花和羊毛
C.用熟石灰区分尿素和氯化铵
D.用燃着的木条区分 二氧化碳和氮气
二氧化碳和氮气
查看答案和解析>>
科目:初中化学 来源: 题型:
现有10.6g碳酸钠和8.4g碳酸氢钠,分别与过量盐酸反应,其中( )
|
| A. | 碳酸钠消耗的氯化氢多 | B. | 碳酸氢钠生成的二氧化碳多 |
|
| C. | 碳酸氢钠消耗的氯化氢多 | D. | 碳酸氢钠生成的二氧化碳多 |
查看答案和解析>>
科目:初中化学 来源: 题型:
硫酸锌溶液可以作木材防腐剂.工业上常用红锌矿(主要是ZnO)和稀硫酸为原料制取硫酸锌,化学反应方程式为:ZnO+H2SO4=ZnSO4+H2O.计算:
(1)硫酸锌中锌元素、硫元素和氧元素间的质量比为 .
(2)如果用100g溶质质量分数为1%的硫酸锌溶液配制10%的硫酸锌溶液,需要加入多少克硫酸锌固体.
(3)取50kg某红锌矿与足量稀硫酸充分反应,最后得到80.5kg硫酸锌,则红锌矿中氧化锌的质量分数是多少?(假设红锌矿中的杂质不与稀硫酸反应)
查看答案和解析>>
科目:初中化学 来源: 题型:
氮化铝(AlN)被广泛应用于集成电路生产领域.在氮气(N2)流中由氧化铝与焦炭在高温条件下制得氮化铝:Al2O3+N2+3C 2AlN+3CO.若有14kg的氮气参加反应,可生成氮化铝的质量为多少?
2AlN+3CO.若有14kg的氮气参加反应,可生成氮化铝的质量为多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
实验室有一瓶长期存放的固体氢氧化钠,由于保管不当已经变质.某兴趣小组的同学欲通过实验测定其变质的情况.实验过程如下,取样品25g放入烧杯中,向其中加入280g过量的稀盐酸,得到296.2g溶液.试计算25g样品中碳酸钠的质量.
查看答案和解析>>
科目:初中化学 来源: 题型:
在氯酸钾里加入了少量的高锰酸钾后,加热时制取氧气的速率大大加快,其主要原因是( )
A.高锰酸钾比氯酸钾容易分解
B.高锰酸钾起了催化作用
C.高锰酸钾受热分解,使产生的氧气增多
D.高锰酸钾受热分解生成的二氧化锰成为氯酸钾受热分解时的催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com