
【题目】甲和乙在一定条件下反应生成丙和丁。结合微观示意图回答下列问题:
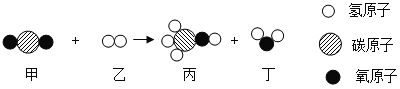
(1)丙中碳氢元素的质量比为__________。
(2)标出丁中氧元素的化合价________。
(3)该反应涉及的四种物质中有________种氧化物。
(4)该化学反应中的最小微粒是_______(选填“分子”或“原子”)。
(5)该反应的化学方程式为________。
【答案】3:1 ![]() 2 原子 CO2+3H2
2 原子 CO2+3H2 CH3OH+H2O
CH3OH+H2O
【解析】
(1)由图可知,丙的分子构成为CH3OH,根据化合物中各元素的质量比等于相对原子质量与原子个数的乘积比可知,丙中碳氢元素的质量比为:3:1,故填写:3:1;
(2)由图可知,丁的分子构成为H2O,已知化合物中氢元素的化合价为+1,根据化合物中,正负化合价代数和为零原则,假设H2O中氧元素的化合价为x,x+(+1)![]() 2=0,则x=-2,故填写:
2=0,则x=-2,故填写:![]() ;
;
(3)由图可知,甲物质的化学式为:CO2,乙物质的化学式为:H2,丙物质的的化学式为:CH3OH,丁物质的化学式为:H2O,根据氧化物是有两种元素组成,其中一种是氧元素的化合物可知,甲和丁属于氧化物,故填写:2;
(4)由图可知,构成甲、乙、丙、丁的圆的形状,化学反应前后没变,而这些圆在图中代表的是原子,因此,该化学反应中的最小微粒是原子,故填写:原子;
(5)该反应是二氧化碳和氢气一定条件下反应生成甲醇和水,化学方程式为:CO2+3H2 CH3OH+H2O,故填写:CO2+3H2
CH3OH+H2O,故填写:CO2+3H2 CH3OH+H2O。
CH3OH+H2O。


科目:初中化学 来源: 题型:
【题目】如图是某食品包装中的干燥剂。

下面是兴趣小组对干燥剂的探究过程,请参与到其中去,回答下列有关问题:
(1)干燥剂能吸水的原因是_____(用化学方程式表示)。
(2)同学们对放置一段时间干燥剂的成分进行探究
(提出问题)干燥剂现在的成分是什么?
(猜想)猜想1:含有CaO 猜想2:含有Ca(OH)2 猜想3:含有CaCO3
(进行实验)
实验步骤 | 实验现象 | 结论 |
1.取少量干燥剂于试管中,向试管中加入少量的水,用手触摸试管外壁 | 试管外壁有热感 | 含有_____ |
2.向步骤1加水后的试管中滴入无色酚酞试液 | 无色酚酞试液变红色 | 含有Ca(OH)2 |
3.向步骤2反应后的试管中加入足量的______ | _____ | 含有CaCO3,反应的化学方程式是______ |
(实验分析)小明同学认为步骤2不能确定Ca(OH)2是否存在,原因是_____。
(改进实验)小明同学进行下列实验

根据小明的实验结果,干燥剂中含有的物质是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定空气中氧气的含量,某兴趣小组的同学选用了40mL的试管作反应容器(如图)和量程体积足够大且润滑效果很好的针筒注射器,将足量的白磷(其化学性质与红磷相似,40℃时就可以燃烧)放入试管后,用橡皮塞塞紧试管,并夹紧弹簧夹.用酒精灯加热白磷,燃烧结束后,等到试管冷却后松开弹簧夹,观察现象.
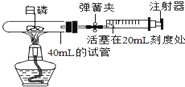
(1)正式开始实验前,该兴趣小组同学打开弹簧夹,将注射器活塞从20ml刻度处推至15ml处,然后松开活塞,观察到活塞返回至20ml刻度处.该操作的主要目的是 。
(2)实验中,在松开弹簧夹前,大试管中可以观察到白磷燃烧发出黄色火焰,并产生 。
(3)实验后,可以观察到针筒活塞会从原来的20mL刻度处慢慢向左移到约( )处.
A.4mL刻度 | B.8mL刻度 | C.12mL刻度 | D.16mL刻度 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是固体物质R在水、酒精两种溶剂中的溶解度曲线。下列说法错误的是( )
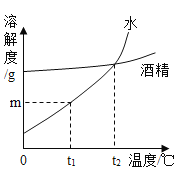
A.R在水中的溶解度受温度影响较大
B.t1 ℃时,R在水中的溶解度为m g
C.t2 ℃时,R在水中与在酒精中的溶解度相等
D.R的饱和水溶液从t1 ℃升温至t2 ℃时,有晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(一)我国化学家侯德榜发明了联合制碱法,其生产纯碱(Na2CO3)和副产品NH4Cl的工艺流程如下(注:NH4Cl的溶解度受温度的影响较大,且随温度的升高而增大):
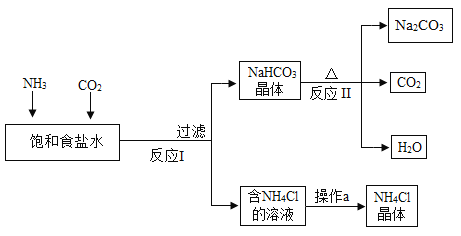
(1)上述工艺流程中可循环利用的物质是_______。
(2)操作a的过程是蒸发浓缩、_______、过滤。
(3)写出反应Ⅰ的化学方程式_______。
(二)下图表示A~H物质间的转化关系。已知A、C、F是单质,D、E是组成元素相同的气体氧化物;H溶液呈蓝色,溶质由两种元素组成;G是赤铁矿的主要成分。
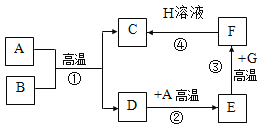
(1)A、H分别是_______、_______(填化学式)。
(2)①~④中,属于置换反应的是_______(填序号),属于化合反应的是_______(填序号),反应③的化学方程式为_______。
(3)将片状的固体F插入H溶液中,可观察到的现象是_______。
(4)列举D在生产生活中的一种用途_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业盐酸中通常溶有少量的FeCl3而呈黄色,小红进行了如下实验:取一定质量该工业盐酸,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示。请回答下列问题:
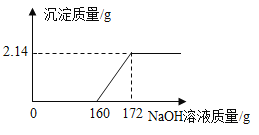
(1)FeCl3与NaOH恰好完全反应时,生成沉淀的质量是 g。
(2)所用NaOH溶液的溶质质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了除去NaCl溶液中含有少量的MgCl2、CaCl2和Na2SO4等杂质,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按一定的顺序进行如图所示的实验。
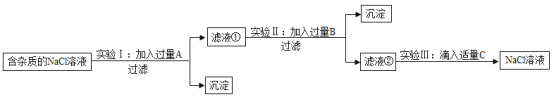
回答下列问题:
(1)实验Ⅰ中加入试剂A除去的杂质是_________。
(2)实验Ⅱ中加入的试剂B是_________溶液;加入过量B的目的是__________。
(3)滤液②中除Na+和Cl-外,还含有的离子是__________(填离子符号)。
(4)实验Ⅲ中发生的中和反应的化学方程式__________。
(5)由所得NaCl溶液制成氯化钠晶体,所需操作为_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图甲是小明在 20℃时进行的系列实验示意图,①-⑤表示实验所得溶液;图乙是 NaCl,KNO3的溶解度曲线(计算均保留一位小数)。
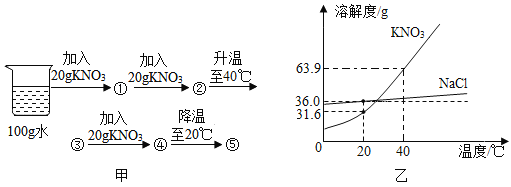
(1)图甲中①溶液的溶质质量分数=__________;①-⑤中属于饱和溶液的是___________;④→⑤的过程中析出 KNO3 晶体__________g。
(2)40℃时,饱和NaCl溶液中溶质的质量分数(w1)与饱和 KNO3溶液中溶质的质量分数(w2)的大小关系是:w1_________w2 (填“>”、“=”或“<”)。
(3)除去KNO3 固体中混有的少量 NaCl 的实验操作是:加适量水溶解→加热得到热饱和溶液→_________→过滤→洗涤→干燥→KNO3 晶体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com