
分析 碳酸钙受热分解生成氧化钙和二氧化碳;
溶液稀释前后,溶质质量不变.
解答 解:(1)设需要石灰石的质量为x,
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,
100 56
x×90% 20t
$\frac{100}{x×90%}$=$\frac{56}{20t}$,
x=39.7t,
故填:39.7.
(2)设需要水的质量为y,
1.84g/cm3×10mL×98%=(1.84g/cm3×10mL+y)×10%,
y=161.92g,
故填:161.92.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | KIO3 | B. | KI | C. | KIO2 | D. | KIO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. |  金属与一定量的稀硫酸反应,若金属M与N在化合物中的化合价都为+2,则相对原子质量M>N | |
| B. | 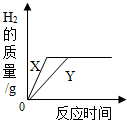 足量金属X与Y与一定量稀硫酸反应,由图象可知金属X比金属Y的活动性更强 | |
| C. |  加热等质量的氯酸钾制取氧气,甲用二氧化锰催化,乙未用二氧化锰催化 | |
| D. | 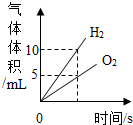 电解水一段时间后,氢气和氧气的体积大小 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 利用太阳能使海水分解来制取氢气 | |
| B. | 加高燃煤锅炉的烟囱,减少污染物的排放 | |
| C. | 了减少水体的污染,农业上禁止使用化肥和农药 | |
| D. | 工业上可制造大量的石灰水,来控制空气中二氧化碳的含量不断上升 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com