
有些同学为图省事常直接喝自来水,更有甚者,剧烈运动之后,开怀畅饮以此为快.这些同学心安理得地认为:自来水消过毒,喝了又何妨.你认为这种说法对吗?自来水应怎样饮用呢?
科目:初中化学 来源: 题型:阅读理解
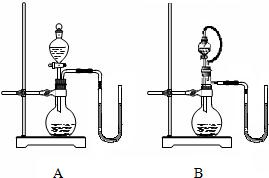 28、物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.
28、物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.查看答案和解析>>
科目:初中化学 来源:新课标新理念新思维人教版化学九年级上册 题型:043
有些同学为图省事常直接喝自来水,更有甚者,剧烈运动之后,开怀畅饮,以此为快.这些同学心安理得地认为:自来水消过毒,喝了又何妨?你认为这种说法对吗?自来水应怎样饮用呢?
查看答案和解析>>
科目:初中化学 来源:化学教研室 题型:043
有些同学为图省事直接喝自来水,更有甚者在剧烈运动之后开怀畅饮,以此为快.这些同学心安理得地认为:自来水消过毒,喝了又何妨.你认为这种说法正确吗?自来水应怎样饮用?
查看答案和解析>>
科目:初中化学 来源: 题型:038
有些同学为图省事直接喝自来水,更有甚者在剧烈运动之后开怀畅饮,以此为快.这些同学心安理得地认为:自来水消过毒,喝了又何妨.你认为这种说法正确吗?自来水应怎样饮用?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com