
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
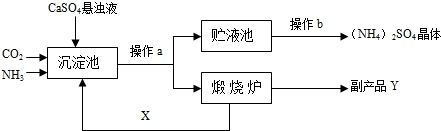
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 溶解度/g | 70.6 | 73 | 75.4 | 78 | 81 | 85 | 88 | ? | 95 | 98 | 103 |
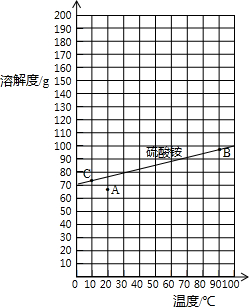
| 指标项目 | 优等品 | 一等品 | 合格品 |
| 外观 | 白色结晶,无可见机械杂质 | 无可见机械杂质 | |
| 氮(N)含量 | ≥21.0% | ≥20.7% | ≥20.5% |
| ||
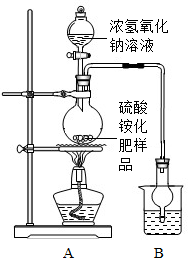
查看答案和解析>>
科目:初中化学 来源: 题型:
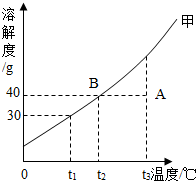
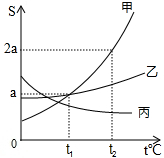 如图是甲、乙、丙三种固体物质的溶解度曲线,请回答:
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:
 水是重要的自然资源,在进行化学实验和溶液中都需要水.请按要求回答下列问题:
水是重要的自然资源,在进行化学实验和溶液中都需要水.请按要求回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com