
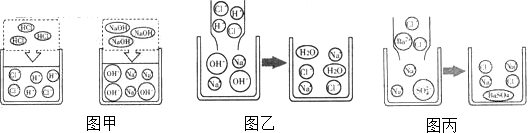
分析 复分解反应的条件是:生成物中有沉淀生成、或有水生成、或有气体冒出;硫酸钠溶液能导电,原因是硫酸钠溶于水,能电离出钠离子和硫酸根离子;氢氧化钠溶液与盐酸反应生成氯化钠和水,实质上氢离子和氢氧根离子生成水分子;硫酸钠溶液跟氯化钡溶液反应生成硫酸钡白色沉淀和氯化钠,配平即可,反应能进行的原因是溶液中Ba2+和SO42-的数目减少.Na2CO3和HCl的实质是:氢离子和碳酸根离子生成水和二氧化碳.复分解反应能发生的本质原因是:溶液中自由移动的离子的数目减少.
解答 解:【迁移运用】硫酸钠溶液能导电,原因是硫酸钠溶于水,能电离出钠离子和硫酸根离子,所以:2Na++SO42-
【分析归纳】
(1)氢氧化钠溶液与盐酸反应生成氯化钠和水,实质上氢离子和氢氧根离子生成水分子;方程式为:NaOH+HCl=NaCl+H20
(2)硫酸钠溶液跟氯化钡溶液反应生成硫酸钡白色沉淀和氯化钠,配平即可,反应的化学方程式是:BaCl2+Na2SO4=BaS04↓+2NaCl,;反应的实质:Ba2++SO42-→BaS04 反应能进行的原因是溶液中钡离子和硫酸根离子的数目减少;
(3)Na2CO3和HCl的实质是:氢离子和碳酸根离子生成水和二氧化碳,反应的实质是:2H++CO32-→H20+CO2↑
【总结规律】复分解反应能发生的本质原因是:溶液中自由移动的离子的数目减少.
故答为:【迁移运用】2Na++SO42-
【分析归纳】(1)NaOH+HCl=NaCl+H20 (2)BaCl2+Na2SO4=BaS04↓+2NaCl,Ba2++SO42-→BaS04,钡离子和硫酸根离子;(3)H20+CO2↑.
【总结规律】溶液中自由移动的离子的数目减少.
点评 本考点考查了复分解反应的实质、实验设计和化学方程式的书写,有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;书写化学方程式要注意配平.本考点主要出现在实验题中.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:初中化学 来源: 题型:解答题
 实验室按图所示装置制取CO2,并试验CO2的性质,试回答以下问题:
实验室按图所示装置制取CO2,并试验CO2的性质,试回答以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 全部正确 | B. | 仅①③④正确 | C. | 仅①正确 | D. | 仅②③正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子可由原子构成,所以原子的体积比分子小 | |
| B. | 分子可以保持物质的化学性质,而原子不能 | |
| C. | 分子在永不停息地做无规则运动,而原子不能 | |
| D. | 化学反应中,分子可以再分,而原子不能再分 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | -5 | B. | -3 | C. | +3 | D. | +5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com