
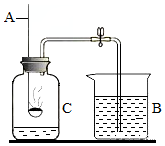
 如图为探究空气中氧气含量的实验:
如图为探究空气中氧气含量的实验:分析 根据红磷在燃烧时的主要现象是:放热,产生大量白烟解答;根据红磷的燃烧结合压强知识分析,红磷与氧气反应生成固体,消耗了瓶内的气体,压强减小,外界大气压会压着水进入集气瓶解答;红磷在空气中燃烧生成五氧化二磷;剩余的气体主要包括氮气和稀有气体等不支持燃烧的气体以及该实验的注意事项进行解答.保证本实验成功的关键是:①装置气密性好;②红磷要足量;③要冷却至室温再读数.
解答 解:
(1)红磷在燃烧时的主要现象是:放热,产生大量白烟;红磷与氧气反应,生成了五氧化二磷固体,所以会导致集气瓶内压强减小,水被压入集气瓶,进入的水量正好占据集气瓶内氧气的空间,约为集气瓶体积的五分之一;
(2)图中所示,进入水的体积约占瓶内容积的$\frac{1}{5}$,说明被消耗的氧气占空气体积的$\frac{1}{5}$;
(3)红磷燃烧把氧气耗尽,就不再燃烧,剩余的成分主要是氮气,说明了氮气不能燃烧,也不能支持燃烧;水被倒吸入集气瓶中,剩余的气体中还主要是氮气,说明氮气难溶于水(合理即可).
(4)由分析可知,造成测得的氧气体积分数小于1/5结果的可能原因:①红磷的量不足; ②装置漏气(如塞子未塞紧、燃烧匙与橡皮塞之间有缝隙等),使外界空气进入瓶内; ③未冷却至室温就打开弹簧夹,使进入瓶内的水的体积减少,
故答案为:
(1)大量白烟;烧杯中的水倒吸入集气瓶,占瓶中约五分之一的体积;
(2)氧气约占空气体积的$\frac{1}{5}$;
(3)氮气;氮气不能燃烧、不能支持燃烧;氮气难溶于水等(合理即可)
(4)装置漏气;红磷的量不足(或未冷却至室温就打开弹簧夹).
点评 本题通过考查用红磷测定氧气在空气中含量的实验的注意事项,学会实验数据的处理或者误差分析的方法及技巧.


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:初中化学 来源: 题型:选择题
| A. | 活性炭用于净水 | B. | 焦炭用于冶炼金属 | ||
| C. | 钨用于制灯泡中的灯丝 | D. | 液氮用于医疗上冷冻麻醉 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷在空气燃烧时出现大量白烟 | B. | 镁带在空气中燃烧生成氧化镁 | ||
| C. | 铁丝在空气中剧烈燃烧,火星四射 | D. | 硫在空气中燃烧火焰呈蓝紫色 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 发展氢能和太阳能 | B. | 限制塑料制品的使用 | ||
| C. | 提高原子利用率,发展绿色化学 | D. | 尽量用纯液态有机物代替水作溶剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. |  加热一定量的高锰酸钾固体 | |
| B. |  向一定量的二氧化锰中加入过氧化氢溶液 | |
| C. |  用等质量氯酸钾制取氧气 | |
| D. |  将水通电电解一段时间 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 67 |

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题


| 实验操作 | 实验现象 | 实验结论 |
| ①取少量4号溶液于试管中,加入足量CaCl2溶液. ②向上层清液中滴加无色酚酞溶液. | ①有白色沉淀生成 ②溶液由无色变成红色 | 4号溶液是部分变质的NaOH溶液. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com