
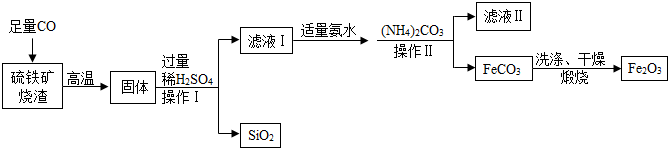
分析 根据已有的物质的性质进行分析解答,过滤是分离不溶性固体和液体的方法,根据过滤用到的玻璃仪器进行解答;一氧化碳能将氧化铁还原为铁,将氧化亚铁还原为铁,故硫铁矿高温通入一氧化碳得到的固体中主要含有的是铁,稀硫酸能与铁反应生成硫酸亚铁和氢气,氨水呈碱性,能够与酸反应;根据反应物和生成物确定反应的化学方程式,据此解答.
解答 解:(1)据图可以看出,经过操作Ⅰ、操作Ⅱ得到的是滤液和固体,故是过滤操作,用到的玻璃仪器有玻璃棒、烧杯、漏斗,故填:漏斗.
(2)一氧化碳能将氧化铁还原为铁,将氧化亚铁还原为铁,故硫铁矿高温通入一氧化碳得到的固体中主要含有的是铁,稀硫酸能与铁反应生成硫酸亚铁和氢气,故含有亚铁离子,由于硫酸过量,故含有氢离子,滤液Ⅰ中主要的阳离子是亚铁离子和氢离子,故填:Fe2+、H+.
(3)由于硫酸过量,溶液呈酸性,氨水呈碱性,加适量氨水能除去过量的硫酸,将溶液调节为中性,故填:除去过量的硫酸,调节溶液的酸碱性.
(4)碳酸铵能与硫酸亚铁反应生成碳酸亚铁和硫酸铵,故滤液Ⅱ中可回收的产品是硫酸铵,故填:(NH4)2SO4.
(5)在空气中煅烧FeCO3生成氧化铁和二氧化碳,反应的化学方程式是:4FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4CO2.故填:4FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4CO2.
点评 本题考查的是常见的物质制备和分离的知识,完成此题,可以依据已有的知识进行,要熟练掌握有关物质的化学性质,以便灵活应用.


科目:初中化学 来源: 题型:解答题
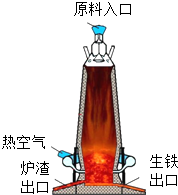 钢铁的生产和使用是人类文明和社会进步的一个重要标志.从2002起,我国的钢铁产量连续多年保持世界第一.如图的设备可用于工业炼铁.
钢铁的生产和使用是人类文明和社会进步的一个重要标志.从2002起,我国的钢铁产量连续多年保持世界第一.如图的设备可用于工业炼铁.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 现象 | 结论 | |
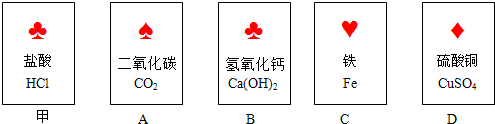
| 甲 | 取少量固体C,溶于适量水形成溶液后,滴加几滴酚酞试液 | 溶液变红 | 猜想成立 |
| 乙 | 取少量固体C,溶于适量水形成溶液后,滴加足量稀盐酸 | 无气泡产生 | 猜想不成立 |
| 丙 | 取少量固体C,溶于适量水形成溶液后,滴加几滴饱和溶液碳酸钠溶液 | 生成白色沉淀 | 猜想成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 序号 | (1) | (2) | (3) | (4) | (5) |
| 名称 | 亚硫酸 | 氖气 | 碳酸氢铵 | 酒精 | |
| 化学式 | H2SO3 | Fe(OH)2 | NH4HCO3 | C2H5OH | |
| 类别 | |||||
| 化合价 | 0 | +2 | -2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com