在高效复习课堂中,同学们利用“盐酸、硝酸钙、氢氧化钠、碳酸钠”四种物质的溶液对“复分解反应发生的条件”进行再探究.
【知识回放】通过判断上述四种溶液两两之间能否发生反应,若能写出其中符合下列条件的两个化学方程式:
(1)一个中和反应
HCl+NaOH═NaCl+H2O
HCl+NaOH═NaCl+H2O
;
(2)一个有沉淀生成的反应
Na2CO3+Ca(NO3)2═CaCO3↓+2NaNO3
Na2CO3+Ca(NO3)2═CaCO3↓+2NaNO3
.
【挖掘实质】
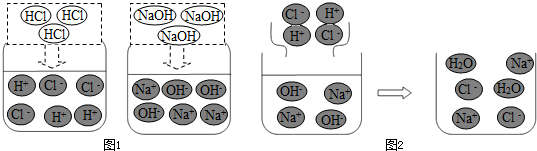
(1)图1是HCl和NaOH在水中解离出离子的示意图,小丽发现HCl在水中会解离出H
+和Cl
-,NaOH在水中会解离出Na
+和OH
-,以此类推硝酸钡在水中会解离出的离子是
Ba2+和NO3-
Ba2+和NO3-
(填离子符号).
(2)图2是稀盐酸和氢氧化钠溶液发生化学反应的微观过程示意图,该化学反应的实质可以表示为 H
++OH
-=H
2O,我也能用同样的方式表示上述四种溶液两两之间发生反应时有气体生成的反应的实质
2H++CO32-═H2O+CO2↑
2H++CO32-═H2O+CO2↑
.
【实践运用】
通过上述探究发现,在溶液中H
+和OH
-不能大量共存,我还发现在溶液中
Ca2+
Ca2+
和
CO32-
CO32-
(填离子符号)也不能大量共存.

