
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |
 |
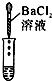 |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 有气泡产生 |
产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |

| 80 |
| 20g×10% |
| 142 |
| x |
| 14.2g-3.55g |
| 100g |
| 142 |
| y |
| 233 |
| 23.3g |
| 14.2g-3.55g |
| 100g |


科目:初中化学 来源: 题型:阅读理解
| 实验方案 | a.测溶液pH | b.滴加Na2CO3溶液 | c.滴加BaC12溶液 |
| 实验操作 |  |
 |
 |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 有气泡产生 有气泡产生 |
产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验方案 | 测溶液的pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |
 |
 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 有气泡产生 |
产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 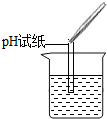 |
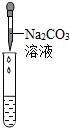 |
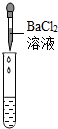 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 测溶液的pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | ______ | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com