
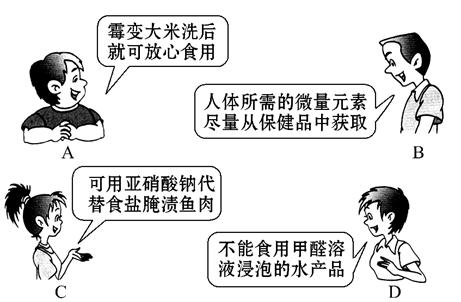
下面是4位同学对“化学与健康”这一话题发表的见解,其中正确的是( )
科目:初中化学 来源: 题型:
A元素的原子结构示意图为: A元素在化学反应中容易 电子变成________离子,属于_________元素(填金属或非金属);B元素的离子结构示意图为: ,该离子带______个单位正电荷,该元素的原子核外总共有_______个电子。A、B元素形成化合物的化学式(用A、B表示)为_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
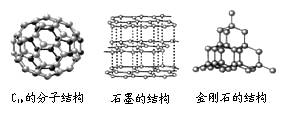
如右下图所示三种物质的物理性质(填:有、无) 差异。你在初中化学中先后接触到以下几组物质:O2和O3;红磷和白磷;金刚石、石墨和C60。由此可以得出的结论是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
用图2所示装置研究“活性炭吸附能力与温度变化的关系”。将NH4NO3固体加入到水中搅拌,观察到两侧玻璃管中液面上升的高度不同。
(1)由于试管内气体的压强 (选填“增大”或“减小”),使得玻璃管内液面上升。
(2)NH4NO3固体溶于水 (选填“放出”或“吸收”)热量。
(3)活性炭吸附气体的能力随温度 而增强。
查看答案和解析>>
科目:初中化学 来源: 题型:
 使用下列方法处理过的食品,不会危及人体健康的是( )
使用下列方法处理过的食品,不会危及人体健康的是( )
A.添加大量防腐剂的肉类制品
B.添加工业明胶的老酸奶、果冻
C.用福尔马林(甲醛的水溶液)浸泡的海鲜
D.包装袋中充入氮气的食品
查看答案和解析>>
科目:初中化学 来源: 题型:
重金属盐可使人中毒,当人误食重金属盐时,可以喝大量牛奶、鸡蛋清或豆浆解毒。原因是上述物质中含有较多的蛋白质,蛋白质可以和重金属盐形成不溶于水的化合物,可以减少重金属盐类对胃肠粘膜的危害,起到缓解毒性的作用,为了验证蛋白质与重金属盐类反应,形成难溶于水的化合物,我们可以做如下实验:
在一支试管中加入3 mL鸡蛋清溶液,再加少量的乙酸铅溶液,然后把试管中的物质倒入盛有清水的小烧杯中观察现象并回答问题:
(1)小烧杯中出现的现象
。
(2)为什么在农业上可以用硫酸铜配制的波尔多液来消灭害虫?
查看答案和解析>>
科目:初中化学 来源: 题型:
通过下列实验操作和现象能得出相应结论的是( )
| 实验操作 | 现象 | 结论 | |
| A | 向收集满CO2的软塑料瓶中加入约1/3体积的NaCl溶液,旋紧瓶盖,振荡 | 塑料瓶变瘪 | CO2能与NaCl反应 |
| B | 50℃时,将17gKCl固体加入50g蒸馏水中,完全溶解后缓慢降温 | 降温至20℃时开始有晶体析出 | 20℃时,KCl的溶解度为17g |
| C | 将白磷浸没在热水中,再向热水中的白磷通氧气 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 氧气是燃烧需要的条件之一 |
| D | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体是CH4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
为探究气体X的组成,某兴趣小组进行图所示实验(固定装置未画出)。
【资料在线】
(1)加热条件下,气体X能与氧化铜反应生成铜、水和氮气。
(2)碱 石灰为固体氢氧化钠和氧
石灰为固体氢氧化钠和氧 化钙的混合物,不与气体X反应。无水氯化钙可吸收气体X。
化钙的混合物,不与气体X反应。无水氯化钙可吸收气体X。
(3)本实验条件下,氮气密度为1.15g·L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计。
【实验步骤】
(1)连接仪器,并检查装置气密性。
(2)取一定量氧化铜,准确称得其质量为2.40g。
(3)按图所示装入药品,测量并记录相关数据Ⅰ(见表)。
(4)连接A、B、C装置, 将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热。当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表)。
【实验装置】

【相关数据】
| 测量项目 数据编号 | I | II |
| 玻璃管(含药品)的质量/g | 52.40 | 51.92 |
| B装置(含药品)的质量/g | 102.00 | 102.54 |
| 氮气的体积/mL | 243.5 |
【回答问题】
⑴B装置中氧化钙吸水的原理为 (用化学方程式表示)。
⑵实验过程中,当观察到 ,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是 。
⑶分析 实验测量的数据,生成水的质量为 g,氧化铜中氧元素的质量为 g。由此推知,气体X中一定 (填“有”或 “没有”)氧元素。
实验测量的数据,生成水的质量为 g,氧化铜中氧元素的质量为 g。由此推知,气体X中一定 (填“有”或 “没有”)氧元素。
⑷通过计算推导出气体X的化学式。
查看答案和解析>>
科目:初中化学 来源: 题型:
在一堂化学实验课上,老师为每组同学分别提供了一瓶氢氧化钠溶液,让他们用1%的稀盐酸来测定其溶质的质量分数。以下是几组同学的设想及做法:
|
 |
请回答:
①酚酞溶液的作用是 ▲ ;
②边滴加稀盐酸,边要用玻璃棒不断搅拌的目的是 ▲ 。
③当溶液颜色恰好变为无色时,共用去了稀盐酸7.3g,则甲组这瓶氢氧化钠溶液中溶质的质量分数为 ▲ (写出计算过程,结果用百分数表示)。
(2)乙组同学的设想是:在烧杯中加入一定量的氢氧化钠溶液,用滴管慢慢滴入1%的稀盐
酸,并不断搅拌,通过用pH试纸多次测定溶液pH的办法,达到实验目的。
①下列使用pH试纸的方法正确的是 ▲ (填字母)。
A.将pH试纸剪成几段节约使用
B.将pH试纸直接插入待测液中
C.将pH试纸放在干净的白瓷板上,用玻璃棒蘸取待测液滴在pH试纸上
D.将pH试纸润湿后放在玻璃片上,用玻璃棒蘸取待测液滴在pH试纸上
 ②由于用pH试纸需多次测定,较繁琐,且所测数值不够精确。在老师指导下,乙组同学取了5g氢氧化钠溶液进行了数字化实验,由计算机描绘出了整个实验过程中溶液pH的变化图像(简单表示为下图)。
②由于用pH试纸需多次测定,较繁琐,且所测数值不够精确。在老师指导下,乙组同学取了5g氢氧化钠溶液进行了数字化实验,由计算机描绘出了整个实验过程中溶液pH的变化图像(简单表示为下图)。
请回答:图中a点表示的含义是 ▲ ;b点溶液中含有的阳离子有 ▲ (填离子符号);乙组同学要计算出本组这瓶氢氧化钠溶液中溶质的质量分数,除了要用到已有数据外,你认为还需要的数据是 ▲ 。
(3)丙组同学在滴加稀盐酸一段时间后,发现溶液中有少量气泡产生。这一“异常现象”激起了他们的探究欲望, 通过实验证明:该组用的这瓶氢氧化钠溶液已经部分变质。
通过实验证明:该组用的这瓶氢氧化钠溶液已经部分变质。
请用化学方程式表示其变质的原因 ▲ ;若要除去溶液中变质生成的杂质,请简要写出你的实验方案: ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com