
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学实验 | 取中和反应后溶液少许于试管中,向试管中滴加几滴无色酚酞溶液 | 溶液变红色 | 猜想(3)成立 |
分析 【作出猜想】根据硫酸和氢氧化钠反应生成硫酸钠和水,两种物质可能恰好完全反应,也可能其中的一种物质过量进行分析;
【实验验证】根据氢氧化钠溶液显碱性,能使酚酞变红色进行分析;
【总结反思】根据氢氧化钠和硫酸反应生成硫酸钠和水,不能共存进行分析;
【知识拓展】(1)根据Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质进行分析;
(2)根据铝和氢氧化钠反应会生成偏铝酸钠和氢气,氢气具有可燃性进行分析;
(3)根据铝和硫酸会制得氢气进行分析;根据反应物、生成物的反应类别判断反应的基本类型
解答 解:【作出猜想】硫酸和氢氧化钠反应生成硫酸钠和水,两种物质可能恰好完全反应,也可能其中的一种物质过量,所以乙同学认为溶液中的溶质是Na2SO4和硫酸两种物质;
【实验验证】氢氧化钠溶液显碱性,能使酚酞变红色,所以取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液,溶液变红色,猜想(3)成立
【总结反思】氢氧化钠和硫酸反应生成硫酸钠和水,不能共存,所以丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是:滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸;
【知识拓展】(1)Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质,所以生活中不能用铝制品来盛放强碱性溶液;
(2)铝和氢氧化钠反应会生成偏铝酸钠和氢气,氢气具有可燃性,所以乙同学的实验中铝片与氢氧化钠溶液发生了反应,铝与氢氧化钠溶液发生反应生成偏铝酸钠和氢气,化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
(3)铝和硫酸反应生成硫酸铝和氢气,方程式为:2Al+3H2SO4=Al2(SO4)3+3H2↑;该反应由一种单质与一种化合物反应生成另一种单质和另一种化合物,符合置换反应的概念,属于置换反应;
故答案为:
【作出猜想】(2)H2SO4;
【实验验证】红;
【总结反思】滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸;
【知识拓展】(1)不能;
(2)NaOH;
(3)2Al+3H2SO4=Al2(SO4)3+3H2↑;置换;
点评 对反应后溶液组成成分进行猜想时,可根据反应物恰好完全反应或反应物之一过量进行分析,判断出反应后溶液的可能组成.


 能力评价系列答案
能力评价系列答案科目:初中化学 来源: 题型:选择题
| A. | 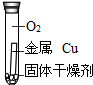 | B. | 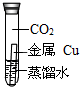 | C. |  | D. | 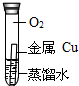 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| ①取白色粉末少量于试管中,加少量的蒸馏水、震荡,发现试管底部有白色固体,取试管中的上层清液,滴加1~2滴无色酚酞试液 | 溶液呈红色 | 白色粉末中 有 Ca(OH)2和CaCO3 |
②往上述试管残留的白色固体中加入稀盐酸 | 有气泡产生 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
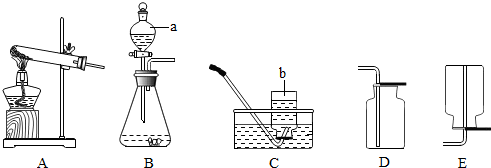
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质用途 | 金刚石切割玻璃 | 石墨作电极 | 活性炭净水 |
| 对应特征 | ①硬度大 | ②导电性好 | ③吸附性好 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com