
| 总热量 | 蛋白质 | 糖类 | 油脂 | 钠 | 维生素C |
| 1016kJ | 5.1g | 11.3g | 19g | 4.6mg | 3.3mg |
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:初中化学 来源: 题型:实验探究题
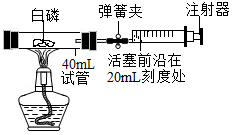 如图所示为测定空气中氧气含量的装置及药品:选用实际容积为40mL的直玻璃管作反应容器,将过量的白磷放入直玻璃管,用橡皮塞塞紧直玻璃管,再与容积为60mL且润滑性良好的针筒注射器组成实验装置.假设此装置能按照设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
如图所示为测定空气中氧气含量的装置及药品:选用实际容积为40mL的直玻璃管作反应容器,将过量的白磷放入直玻璃管,用橡皮塞塞紧直玻璃管,再与容积为60mL且润滑性良好的针筒注射器组成实验装置.假设此装置能按照设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
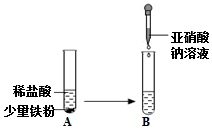 亚硝酸钠(NaNO2)是一种淡黄色或白色晶体,有咸味,易潮解,易溶于水,其水溶液呈碱性;在320℃时能分解产生氧化钠固体、一氧化氮气体和一种常见的助燃性气体.亚硝酸钠有毒性,能将人体血红蛋白中的+2价亚铁离子转化为+3价铁离子,使血红蛋白失去携氧能力,因此误服亚硝酸钠会使人中毒.
亚硝酸钠(NaNO2)是一种淡黄色或白色晶体,有咸味,易潮解,易溶于水,其水溶液呈碱性;在320℃时能分解产生氧化钠固体、一氧化氮气体和一种常见的助燃性气体.亚硝酸钠有毒性,能将人体血红蛋白中的+2价亚铁离子转化为+3价铁离子,使血红蛋白失去携氧能力,因此误服亚硝酸钠会使人中毒.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盐 盐 酸 碱 | B. | 盐 酸 酸 碱 | ||
| C. | 盐 盐 酸 盐 | D. | 碱 盐 酸 盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | b>50 | B. | b<50 | C. | b≥50 | D. | b≤50 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
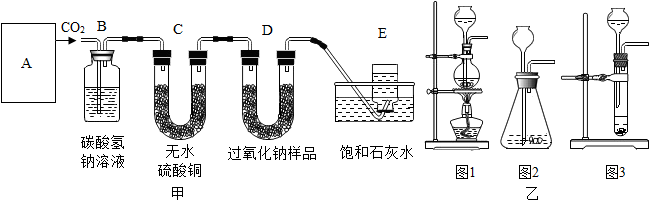
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
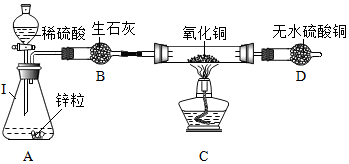
| 操作 | 判断依据 | 结论 | |
| 方案一 | 用试管取少量C中反应后的物质,向其中滴加稀盐酸(或稀硫酸),振荡,观察现象 | 溶液变蓝色 (或溶液未变蓝色) | 氧化铜未消耗完 (氧化铜基本消耗完) |
| 方案二 | 称量反应后C中剩余固体的质量 | 剩余固体的质量约为3.2g (或剩余固体的质量大于3.2g) | 氧化铜基本消耗完 (氧化铜未消耗完) |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com