
【题目】A、B、C 三种固体物质在水中的溶解度曲线如图 1 所示,请回答:
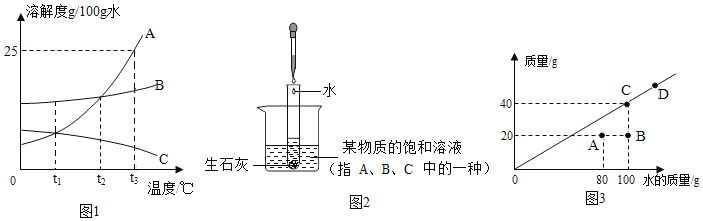
①_____℃时,A、B 两种物质溶解度相等;
②t3℃时恰好溶解掉等质量的 A、B、C 三种物质,所消耗的水最多的是_____;
③若将 t3℃三种物质的饱和溶液分别降温 t1℃时,则对三种溶液的说法正确 的是_____;
A 溶剂质量:C>B>A B 都是饱和溶液
C 溶质质量分数:B>A>C D 析出溶质的质量:B>A>C
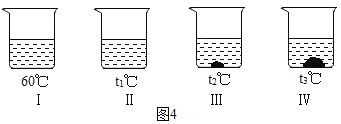
④图 2 所示,向盛有生石灰的试管中加入适量水,反应的化学方程式 是_____。实验时,烧杯中有固体析出,判断该饱和溶 液中析出的晶体是_____(填 A 或 B 或 C)。
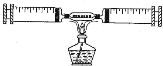
⑤常温时,某物质在不同质量的水中溶解达到饱和状态,溶质的质量与水的质量关系如图所示。
a.常温时,该物质的溶解度是_____
b.A 点时,该溶液的溶质质量分数为_____
c.图中 A、B、C、D 四个点表示的溶液中溶质质量分数从大到小的关系是_____
⑥向不同温度的 100g 水中分别放入等质量的某物质,保持温度不变,溶解情况如图4所示。相关分析正确的是_____。
a.溶液温度:Ⅰ>Ⅱ>Ⅲ>Ⅳ
b.溶液质量:Ⅰ=Ⅱ>Ⅲ>Ⅳ
c.溶液Ⅰ一定是不饱和溶液
d.使Ⅳ中的固体全部溶解,溶质质量分数可能不变
【答案】t2 C C CaO+H2O=Ca(OH)2 C 40g 20% C=D>A>B bd
【解析】
①在t2℃时,A、B 两种物质溶解度相等;
②t3℃时恰好溶解掉等质量的 A、B、C 三种物质,所消耗的水最多的是C,因为在该温度下C的溶解度最小;
③若将t3℃三种物质的饱和溶液分别降温t1℃时,则对三种溶液的说法正确的是溶质质量分数:B>A>C,因为C的质量分数不变,还是最小;
④图2所示,向盛有生石灰的试管中加入适量水生成氢氧化钙,同时放出大量的热,反应的化学方程式是:CaO+H2O=Ca(OH)2;实验时,烧杯中有固体析出,判断该饱和溶液中析出的晶体是C,因为C的溶解度随温度升高而降低;
⑤常温时,某物质在不同质量的水中溶解达到饱和状态,溶质的质量与水的质量关系如图3所示;a、常温时,该物质的溶解度是40g;
b、A 点时,该溶液的溶质质量分数=![]()
![]() 100%=20%;
100%=20%;
c、图中 A、B、C、D 四个点表示的溶液中溶质质量分数从大到小的关系是:C=D>A>B;⑥向不同温度的100g水中分别放入等质量的某物质,保持温度不变,溶解情况如图4所示;由于某物质的溶解度随温度变化情况未知,则相关分析正确的是:b、溶液质量:Ⅰ=Ⅱ>Ⅲ>Ⅳ;d、采用增加溶剂的方法使Ⅳ中的固体全部溶解,溶质质量分数可能不变。


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:初中化学 来源: 题型:
【题目】2019年底,徐宿淮盐铁路将建成通车,淮安人可实现高铁出行。
(1)高铁在建造时使用了大量的新材料,下列属于金属材料的是______(填序号)。

A 生产高铁车头的玻璃钢
B 制造高铁车身的镁铝合金
C 制造轨道枕木的聚氨酯材料
D 建筑高铁路基的钢筋混凝土
(2)高铁刹车制动盘使用合金锻钢制作,主要利用该合金耐高温、______等特性。
(3)在高铁站的建设中,使用了大量的钢铁。工业上用赤铁矿(主要成分是氧化铁)和一氧化碳反应冶炼铁,该反应的化学方程式为______。
(4)高铁轨道焊接时,可用铝热反应:2Al+Fe2O3![]() 2Fe+Al2O3,该反应的基本类型是______。
2Fe+Al2O3,该反应的基本类型是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是某同学测定空气中氧气含量的装置,玻璃管中装的是细铜丝。
(已知:铜 +氧气![]() 氧化铜;氧化铜是固体)
氧化铜;氧化铜是固体)
(1)若加热前,两注射器组成的密闭系统中有 30mL 空气,停止加热冷却到室温后,理论上密闭容器中剩余的气体的体积为_____________mL,由此证明空气中氧气约占空气总体积的_____________。
(2)不同的同学在做上述实验时结果差别较大,甲同学最后剩余气体26mL,你认为可能的原因有哪些?
①____________________________________
②__________________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是宝贵的自然资源,是人类生命之源.
(1)为了净化河水,可以向其中添加明矾,明矾的作用是_____;
(2)生活中既可以软化硬水,又可以消毒杀菌的方法是_____;
(3)ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒.制取ClO2的反应过程示意图如下,请回答:

C物质中氯元素的化合价是_____.
(4)水与人类生活息息相关,下列关于水的说法,错误的是_____.(填字母)
A 自然界中的水都是混合物
B 使用无磷洗涤剂有利于防止水体富营养化
C 水电解产生氢气和氧气,说明水分子中含氢分子和氧分子
D 用活性炭除去水中的色素和异味
E 我们把含有较多可溶性钙、镁化合物的水称为硬水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】浓度为 10%的氢氧化钠溶液 100g,如果浓度要增加一倍,应采用( )
A. 将溶液蒸发掉一半
B. 加入 100g10%的氢氧化钠溶液
C. 增加 10g 氢氧化钠固体
D. 溶剂蒸发掉 45g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学家在环境问题上提出的最新构想是变废为宝,资源循环利用。例如将燃料进行如下循环: ![]() ,这样既可解决能源问题,又能消除污染。上述构想中两个转化过程的变化为
,这样既可解决能源问题,又能消除污染。上述构想中两个转化过程的变化为
A. (1)为物理变化,(2)为化学变化B. 均为化学变化
C. (1)为化学变化,(2)为物理变化D. 均为物理变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列装置都可用于测定空气里氧气的含量,a、b两物质的选择正确的是
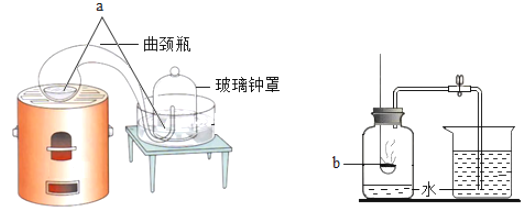
A. a是汞 b是红磷B. a是铁丝 b是硫粉
C. a是汞 b是硫粉D. a是红磷 b是蜡烛
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水污染与防治是当今人类需要关注的环境问题之一,工农业废水和生活污水是水污染的主要来源。回答下列问题:
(1)酸雨________(填“能”或“不能”)污染水体,煤燃烧产生SO2,SO2形成酸雨的主要原因是________。
(2)废旧电池中含有的汞、镉等重金属会污染水体,造成生物体中毒,其原因是重金属能使生物体内的________(填化学物质)结构破坏,失去生理活性。
(3)某工业废水含HgSO4,可通过铁网而将汞留下,加热将汞形成蒸气回收利用。其反应的化学方程式为________,汞的沸点________(填“低于”或“高于”)铁的沸点。也可以向废水中加入Na2S溶液形成沉淀而除去汞,该沉淀的化学式为________。
(4)甲厂污水含硫酸的质量分数为0.98%,其流速为45kg/s,乙厂污水含烧碱的质量分数为0.4%,为排放达标,现将两厂的污水混合处理,反应的化学方程式为________,则乙厂污水的最佳流速为________kg/s。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】无水氯化钙的用途广泛。以石灰石矿粉(含有MgSO4、Fe2O3、SiO2等杂质)为原料,生产无水氯化钙的流程如图:
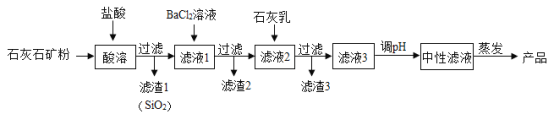
(1)写出过滤操作中用到的任意一种玻璃仪器的名称_____;
(2)写出滤液1中含有的所有金属阳离子的符号_____;
(3)滤渣3中的固体除有Ca(OH)2外,还有_____(写化学式);
(4)对滤液3调节pH值时发生反应的化学方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com