
| 温度/℃ | 10 | 20 | 30 | 40 |
| 溶解度/g | 0.244 | 0.255 | 0.264 | 0.265 |
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度(%) | 15 | 20 | 25 | 30 | 35 |
| 气体体积/mL | 35 | 47 | 55 | 51 | 42 |
| 试管编号 | A | B | C | D | E |
| 温度/℃ | 40 | 50 | 60 | 70 | 80 |
| 现象和 比较 | 有少量气泡 | 气泡比A号试管多 | 气泡明显比B号试管多 | 大量气泡产生,与常温用盐酸反应相似 | 反应非常激烈,迅速产生大量气体 |
分析 (一)
(1)根据浓盐酸具有挥发性解答;
(2)根据碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳解答;
(二)
(3)根据反应生成的硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止解答;
(4)分析实验一中的表格中数据作对比即可得出正确答案;
(5)根据表格中数据作对比即可得出正确答案;
(6)观察实验二中表格中的数据作对比即可得出正确答案;
(7)碳酸钙固体颗粒大小也会影响反应的速率,可以据此解答.
解答 解:
(一)
(1)实验室制取二氧化碳气体选用稀盐酸,而不选用浓盐酸,是因为浓盐酸具有挥发性,否则会造成制取的二氧化碳气体不纯.
(2)用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(二)
(3)实验室不选用稀硫酸制取CO2的原因:反应生成的硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止;
(4)观察实验一中的表格中数据可以知道,3号试管收集的气体最多,此时管中硫酸浓度是25%,浓度大于或小于此浓度值生成的气体体积都少.
(5)另取一支盛有1g直径为2mm大理石的大试管,注入40%的硫酸5mL,15分钟内生成气体的体积<42mL.
(6)观察实验二中表格中的数据,可知应选择最合适的反应温度为70℃,低于70℃时,生成的气体少并且反应慢,高于70℃反应速率过快,不易收集.
(7)碳酸钙固体颗粒大小也会影响反应的速率,根据表格可知是探究碳酸钙固体颗粒大小.分别取1g块状大理石和粉末状大理石于两支试管中,分别加入5mL25%的稀硫酸,比较产生气泡快慢.
答案:
(一)(1)挥发性;(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(二)
(3)反应生成的硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止;
(4)25%;
(5)<;
(6)70;
(7)碳酸钙颗粒大小;分别取1g块状大理石和粉末状大理石于两支试管中,分别加入5mL25%的稀硫酸,比较产生气泡快慢.
点评 本题以实验探究的形式考查稀硫酸与大理石反应的适宜温度和浓度等问题,培养学生的对比能力、提取信息的能力,注意控制变量的使用.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
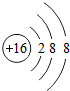 表示的粒子:S;④两个铁离子:2Fe3+;⑤导电、导热性最好的金属:Ag;⑥+2价的镁元素:Mg2+.其中正确的有( )
表示的粒子:S;④两个铁离子:2Fe3+;⑤导电、导热性最好的金属:Ag;⑥+2价的镁元素:Mg2+.其中正确的有( )| A. | ②④⑤ | B. | ①④⑤ | C. | ①③⑤ | D. | ①④⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
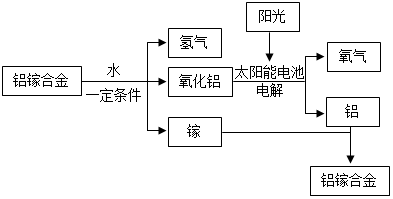
| A. | 铝镓合金可以循环使用 | |
| B. | 太阳能的利用可以部分解决能源危机问题 | |
| C. | 镓铝合金属于化合物 | |
| D. | 铝镓合金与水反应的化学方程式为:2Al+3H2O $\frac{\underline{\;一定条件\;}}{\;}$Al2O3+3H2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
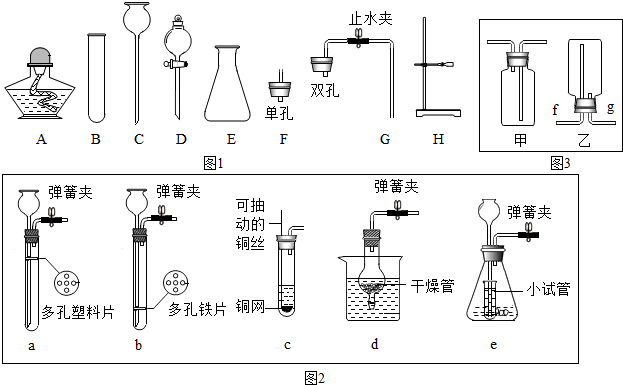
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
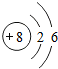 该元素的原子结构示意图如图所示.
该元素的原子结构示意图如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子核内的质子数与其核电荷数相等 | |
| B. | 原子核中的质子数与中子数一定相等 | |
| C. | 原子核一定由质子和中子构成 | |
| D. | 元素的化学性质取决于原子核内的质子数 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com