
���� ��1������̼���������ȷֽ�����̼���ơ�������̼��ˮ�����Լ��ٵ��������Ƕ�����̼�����������ö�����̼���������̼�����Ƶ���������������������NaHCO3�������������ɣ�
��2���������ȷֽ��Ĺ���Ϊ̼���ƹ��壬��������̼���ơ�������̼�Լ�̼��Ƶ�������ϵ��������������������ɣ�
��� �⣺��1����������NaHCO3������Ϊx��
2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2��
168 44
x 0.62g
$\frac{168}{x}=\frac{44}{0.62g}$
x=2.37g
�������NaHCO3����������=$\frac{2.37g}{3.36g}��100%$=70.54%
��2�������ɳ���������Ϊy��
̼���Ƶ�����=3.36g-0.62g=2.74g
Na2CO3+2HCl=2NaCl+H2O+CO2�� CO2+Ca��OH��2=CaCO3��+H2O
Na2CO3 ��CO2 ��CaCO3
106 100
2.74g y
$\frac{106}{2.74g}=\frac{100}{y}$
y=2.58g
�𣺣�1���������NaHCO3����������Ϊ70.54%��
��2�������ȷֽ��Ĺ��������������ᷴӦ����ַ�Ӧ�����ɵ�����ͨ�뵽�����ij���ʯ��ˮ�У���������������Ϊ2.58g��
���� �����ǶԻ�ѧ����ʽ����Ŀ��飬����Ĺؼ����ҵ���֪���������������÷�Ӧ���ɶ�����̼����������������ʵ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ��/t | 0 | 5 | 10 | 15 |
| ����/g | 215.2 | 211.4 | 208.6 | 208.6 |
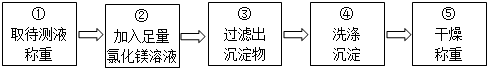
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
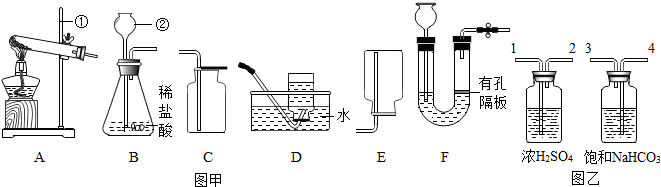
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 2015��3��5Ŀ������Ժ�������ǿ����������������ָ������Ŭ��������̬���������ü����ƹ�����Դ��������
2015��3��5Ŀ������Ժ�������ǿ����������������ָ������Ŭ��������̬���������ü����ƹ�����Դ���������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | 1 | 2 | 3 | 4 |
| ��ϡ���������/g | 14.00 | 14.00 | 14.00 | 14.00 |
| ʣ�����ʵ�����/g | 23.96 | 37.92 | 51.88 | 65.88 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
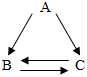 ABC�������ʻ������֮���ת����ϵ����ͼ��ʾ�����ش�
ABC�������ʻ������֮���ת����ϵ����ͼ��ʾ�����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ�鲽�� | �۲쵽������ | ���ۻ���� |
| ��1������ˮ���ռ����� ������������ƿ��װ��ˮ���ò���Ƭ��סƿ�ڣ�������ˮ�У������Ϲ�С�ĵز��뼯��ƿ�ڴ����� �ڼ���ƿ��װ��������ò���Ƭ��סƿ�ڣ���ˮ��ȡ������������ | ����ƿ�е�ˮ���٣����ռ���ƿ�ڳ������������� ˮȫ���ų� | ���������岻�ܣ�ѡ��ܡ����ܡ�����ˮ |
| ��2������Ŀ����ͺ�������������ʱȽ� ����һ��ʢ�����ļ���ƿ��һ��ʢ��������ļ���ƿ�У���������ͬ�����ij���ʯ��ˮ���� �ڽ�ȼ�ŵ�ľ���ֱ����ʢ�п����ͺ�������ļ���ƿ�� ��ȡһ�����IJ���Ƭ���Ź���������ڿ����е���һ�鲣��Ƭ��Ƚ� | ��ʢ�����ļ���ƿ�ڳ���ʯ��ˮû�����Ա仯��ʢ��������ļ���ƿ�ڳ���ʯ��ˮ����� ��ʢ��������ļ���ƿ��ȼ�ŵ�ľ��Ϩ�� �۶��Ź����IJ���Ƭ����ˮ�� | ����������������к��н϶�Ķ�����̼ ����������������к��н��ٵ����� ����������������к��н϶��ˮ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4Fe+3O2$\frac{\underline{\;��ȼ\;}}{\;}$2Fe2O3 | B�� | 2H2+O2$\frac{\underline{\;ͨ��\;}}{\;}$2H2O | ||
| C�� | H2CO3 $\frac{\underline{\;\;��\;\;}}{\;}$H2O+CO2�� | D�� | C2H5OH+O2�TCO2+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
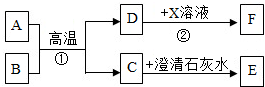
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com