
通过实验对草酸(相对分子质量是90)进行如下研究。
【查阅资料】①浓硫酸常作干燥剂 ②浓NaOH溶液常用于吸收CO2气体
③无水硫酸铜吸水后由白色变为蓝色 ④氯化钯(PdCl2)溶液遇CO产生黑色沉淀
【实验准备】选用下列实验装置(气密性良好,部分固定装置已略去):
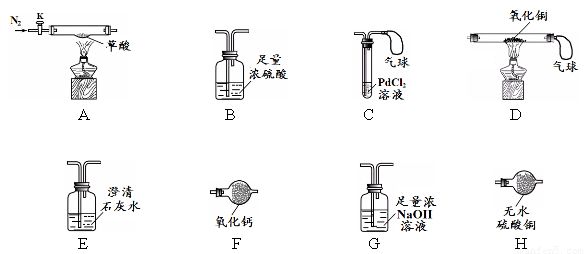
【实验I】检验草酸分解的产物。
|
实验步骤 |
实验现象 |
实验结论及分析 |
|
(1)按A→H→E→C 连接仪器 (2)关闭K,点燃A处酒精灯 |
H中 E中澄清石灰水变浑浊 C中产生黑色沉淀,气球鼓起 |
草酸分解生成了CO2、CO和H2O ①E中反应的化学方程式是 ②C中气球的作用是 |
【实验II】取9 g草酸进行实验,测定生成物的质量并确定草酸的组成。
|
实验步骤 |
实验数据 |
实验结论及分析 |
|
(1)选择A、B、D、G装置组合进行实验 (2)鼓入过量的N2后,分别称量B、D、G的质量 (3)关闭K,点燃A、D处的酒精灯,至草酸完全分解 (4)熄灭A处酒精灯,通入过量的N2,熄灭D处酒精灯,再次分别称量B、D、G的质量 |
B装置增重1.8 g D装置中固体质量减少0.8 g G装置增重4.4 g
|
①A、B、D、G装置的正确连接顺序是A→ → →D ②向A中两次通入N2,其中 第二次的目的是 ③草酸的化学式是 ④反思:若用F代替B,则不能测定草酸的组成,其原因是 |
【实验I】 白色固体变成蓝色 ①CO2 +Ca(OH)2 =CaCO3↓+ H20 ②收集尾气(或尾气处理装置)【实验II】①B→G②将生成的气体完全排入吸收装置,使其被完全吸收③C2H2O4 ④CaO可同时吸收H2O、CO2,导致无法准确测量H2O、CO2的质量
【解析】
试题分析:【实验I】根据实验结论由一氧化碳、二氧化碳和水生成,故看到H干燥管中的硫酸铜由白色变为蓝色;①E中所称药品为氢氧化钙水溶液,故反应的化学方程式是CO2 +Ca(OH)2 =CaCO3↓+ H20 ,②C中气球的作用是收集尾气;【实验II】①A、B、D、G装置的正确连接顺序是A→B → G →D; ②向A中两次通入N2,第一次为了排尽装置内的空气,防止发生爆炸,其中第二次的目的是将生成的气体完全排入吸收装置,使其被完全吸收;
③根据装置质量的变化知道生成水1.8g,一氧化碳得到0.8g氧,生成二氧化碳的质量为4.4g,氢元素的质量为:1.8g×2/18×100%=0.2g;
设草酸分解生成一氧化碳的质量为x,
CO+ CuO Cu
+ CO2
Cu
+ CO2
16
x 0.8g
28:16=x:0.8g
x=1.4g
G吸收二氧化碳共4.4g,所以草酸分解生成的二氧化碳的质量为4.4g
分解的草酸的质量为:4.4g+1.4g+1.8g=7.6g,5.4g草酸中碳元素的质量为1.4g×12/28+4.4g×12/44=0.6g+1.2g=1.8g,所以分解的草酸中氧元素的质量为5.4g-1.2g-0.2g=4g,所以草酸中碳、氢、氧元素的质量比为1.2g:0.2g:4g=6:1:20,设草酸的化学式为CxHyOz则
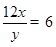 ,
,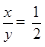 ;
;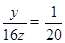 ,
,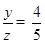
草酸的化学式为C2H2O4
④反思:若用F代替B,则不能测定草酸的组成,其原因是CaO可同时吸收H2O、CO2,导致无法准确测量H2O、CO2的质量
考点:物质的组成


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论及分析 |
| (1)按A→H→E→C 连接仪器 (2)关闭K,点燃A处酒精灯 |
H中 E中澄清石灰水变浑浊 C中产生黑色沉淀,气球鼓起 |
草酸分解生成了CO2、CO和H2O ①E中反应的化学方程式是 ②C中气球的作用是 |
| 实验步骤 | 实验数据 | 实验结论及分析 |
| (1)选择A、B、D、G装置组合进行实验 (2)鼓入过量的N2后,分别 称量B、D、G的质量 (3)关闭K,点燃A、D处的酒精灯, 至草酸完全分解 (4)熄灭A处酒精灯,通入过量的N2, 熄灭D处酒精灯, 再次分别称量B、D、G的质量 |
B装置增重1.8g D装置中固体 质量减少0.8g G装置增重4.4g |
①A、B、D、G装置的正确连接顺序 是A→ ②向A中两次通入N2,其中 第二次的目的是 ③草酸的化学式是 ④反思:若用F代替B, 则不能测定草酸的组成, 其原因是 |
查看答案和解析>>
科目:初中化学 来源:2013年初中毕业升学考试(江苏无锡卷)化学(解析版) 题型:探究题
草酸亚铁晶体(FeC2O4﹒2H2O)是一种浅黄色固体,难溶于水,受热易分解,是生产锂电池的原材料。某化学兴趣小组设计实验验证草酸亚铁热分解的气体产物,并用热重法(TG)确定其分解后固体产物的组成。探究过程如下:
【查阅资料】
1. 草酸亚铁晶体热分解的气体产物是H2O、CO、CO2
2. 白色的无水CuSO4遇水蒸气会变成蓝色
【实验设计】

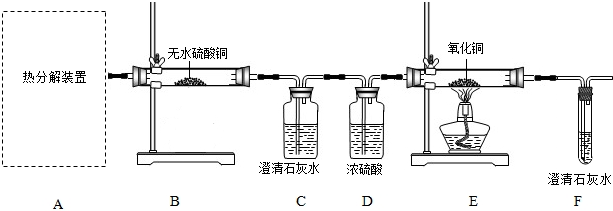
(1)从环保角度考虑,该套实验装置的明显缺陷是 。
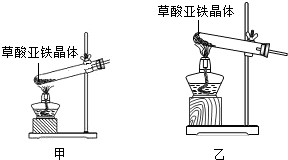
(2)可选择以下实验装置中的 (选填:“甲”或“乙”)作为虚线中的“热分解装置”。

【问题讨论】
(3)D中浓硫酸的作用是 ,实验过程中观察到B中白色无水CuSO4变成蓝色,C中澄清石灰水变浑浊,E中 (填实验现象),则可证明草酸亚铁晶体热分解的气体产物是H2O、CO2、CO。
(4)该兴趣小组进行上述实验时,先点燃热分解装置中的酒精灯,一段时间后再点燃E处的酒精灯,原因是 。
(5)若通过F装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解的气体产物中有CO,则需在C和D装置之间增加盛有 (填物质的名称或化学式)溶液的洗气瓶。
【数据分析】
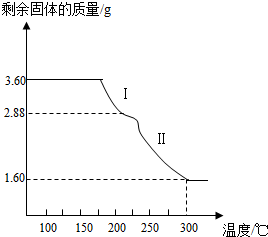
(6)称取3.60g草酸亚铁晶体(FeC2O4﹒2H2O,相对分子质量180)用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如下图所示,请分析该图回答下列问题:

①过程Ⅰ发生反应的化学方程式为 。
②3000℃时剩余固体只有一种且是铁的氧化物,试通过计算确定该氧化物的化学式或名称 。(请写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
通过实验对草酸(相对分子质量是90)进行如下研究。
【查阅资料】①浓硫酸常作干燥剂 ②浓NaOH溶液常用于吸收CO2气体
③无水硫酸铜吸水后由白色变为蓝色 ④氯化 钯(PdCl2)溶液遇CO产生黑色沉淀
钯(PdCl2)溶液遇CO产生黑色沉淀
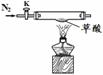
【实验准备】选用下列实验装置(气密性良好,部分固定装置已略去):
 | |||||||
 | |||||||
 |  | ||||||
A B C D
 | |||||||
 | |||||||
 | |||||||
 | |||||||
E F G H
【实验I】检验草酸分解的产物。
| 实验步骤 | 实验现象 | 实验结论及分析 |
| (1)按A→H→E→C 连接仪器 (2)关闭K,点燃A处酒精灯 | H中 E中澄清石灰水变浑浊 C中产生黑色沉淀,气球鼓起 | 草酸分解生成了CO2、CO和H2O ①E中反应的化学方程式是 ②C中气球的作用是 |
【实验II】取9 g草酸进行实验,测定生成物的质量并确定草酸的组成。
| 实验步骤 | 实验数据 | 实验结论及分析 |
| (1)选择A、B、D、G装置组合进行实验 (2)鼓入过量的N2后,分别称量B、D、G的质量 (3)关闭K,点燃A、D处的酒精灯,至草酸完全分解 (4)熄灭A处酒精灯,通入过量的N2,熄灭D处酒精灯,再次分别称量B、D、G的质量 | B装置增重1.8 g D装置中固体 质量减少0.8 g G装置增重4.4 g | ①A、B、D、G装置的正确连接顺序是A→ → →D ②向A中两次通入N2,其中 第二次的目的是 ③草酸的化学式是 ④反思:若用F代替B,则不能测定草酸的组成,其原因是
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com