
 同学们通过查阅资料知道,过氧化氢分解反应的催化剂除二氧化锰外,还有氯化镁溶液、氯化铜溶液中的金属离子和土豆中含有的过氧化氢酶以及氧化铜等.
同学们通过查阅资料知道,过氧化氢分解反应的催化剂除二氧化锰外,还有氯化镁溶液、氯化铜溶液中的金属离子和土豆中含有的过氧化氢酶以及氧化铜等.| 时间/s 试剂 压强/KPa | 0 | 60 | 120 | 180 | 240 | 300 |
| 20mL5%的过氧化氢溶液 | 101.86 | 102.99 | 103.42 | 103.67 | 103.99 | 104.00 |
| 加入氯化铁溶液 | 102.21 | 105.35 | 115.40 | 129.69 | 145.52 | 163.99 |
| 加入氯化铜溶液 | 101.50 | 102.73 | 107.53 | 114.78 | 122.49 | 130.39 |
分析 (1)对比试验中,一定要控制好变量和常量;
(2)根据表中数据可以判断氯化铁溶液和氯化铜溶液对过氧化氢分解的催化效率;
(3)根据实验现象可以判断实验结论;
过氧化氢在催化剂的作用下分解生成水和氧气;
(4)比较过氧化氢分解速率的方法很多,要注意理解;
(5)反应物浓度越大,温度越高,反应速率越快;
(6)过氧化氢溶液的浓度能够影响过氧化氢分解的速率.
解答 解:(1)加入含相同数目金属离子的氯化铁溶液和氯化铜溶液,该步操作的实验目的是:通过对比试验,控制金属离子的数目,对比它们对过氧化氢分解速率的影响.
故填:控制金属离子的数目,对比它们对过氧化氢分解速率的影响.
(2)根据上表数据可知,相同时间内,加入氯化铁粉末的体系压强大于加入氯化铜粉末的体系压强,即相同时间内,加入氯化铁粉末的体系中生成气体的体积大于加入氯化铜粉末的体系中生成气体的体积,因此氯化铁溶液催化产生氧气的速率比氯化铜溶液快;
成若干片的体积比不切的体积大,一段时间后,切成片的土豆片表面附着较多的气泡并不断上升,说明切成片的土豆表面产生的气体多,由此可知,反应物和催化剂的接触面接越大,反应速率越快.
故填:氯化铁溶液催化产生氧气的速率比氯化铜溶液快;反应物和催化剂的接触面接越大,反应速率越快.
(3)过氧化氢在催化剂的作用下分解生成水和氧气的化学方程式为:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
故填:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
(4)A.测量完全反应后产生气体的总体积,能够比较过氧化氢质量的大小,但是不能比较过氧化氢分解的速率,该选项做法不合理;
B.测量产生一定体积气体所需要的时间,可以判断过氧化氢分解的速率快慢,该选项做法合理;
C.测量相同时间内生成气体的体积,可以比较过氧化氢分解的速率大小,该选项做法合理;
D.测量相同时间内锥形瓶内物质总质量的变化,可以判断气体减少的快慢,从而可以判断过氧化氢分解的速率快慢,该选项做法合理.
故填:A.
(5)因为过氧化氢分解时放出热量,导致溶液温度升高,从而加快了过氧化氢的分解.
故填:过氧化氢分解时放出热量,温度升高,反应速率加快.
(6)过氧化氢溶液的浓度能够影响分解速率:
实验步骤:室温下,取相同质量的二氧化锰粉末分别加入两支规格相同的试管中,再分别同时加入相同体积、浓度不同的过氧化氢溶液,连接收集装置;
实验现象:浓度大的过氧化氢溶液产生气泡的速率较快,相同时间内浓度大的过氧化氢溶液收集装置中收集的气体体积大;
实验结论:其它条件相同时,过氧化氢溶液的浓度越大,分解速率越快.
故填:过氧化氢溶液的浓度影响分解速率:
实验步骤:室温下,取相同质量的二氧化锰粉末分别加入两支规格相同的试管中,再分别同时加入相同体积、浓度不同的过氧化氢溶液,连接收集装置;
实验现象:浓度大的过氧化氢溶液产生气泡的速率较快,相同时间内浓度大的过氧化氢溶液收集装置中收集的气体体积大;
实验结论:其它条件相同时,过氧化氢溶液的浓度越大,分解速率越快.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 高楼着火,乘坐电梯逃生 | |
| B. | 被困在火灾区时,用湿毛巾捂住口鼻俯低身子逃生 | |
| C. | 天然气泄露,立即打开换气扇开关 | |
| D. | 炒菜的油锅着火,立即加水灭火 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 送木条是易燃物,硫磺是阻燃物 | B. | “法烛”燃烧会产生刺鼻气味 | ||
| C. | 硫磺降低了松木的着火点 | D. | 吹灭“法烛”是因为隔绝了空气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该反应为分解反应 | B. | 碳铵不属于复合肥料 | ||
| C. | X的化学式NH4 | D. | 碳铵与草木灰等碱性物质不能混用 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 所有化肥都能全部溶于水 | |
| B. | 硝酸钾属于盐,是复合肥料 | |
| C. | 要大量施用化肥才能够获得高产 | |
| D. | 氯化铵与熟石灰混合施用,既能施氮肥又能改良酸性土壤 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
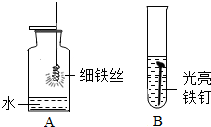 以下是初中化学有关铁的性质的一些基本实验,请回答问题.
以下是初中化学有关铁的性质的一些基本实验,请回答问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com