
【题目】久置的铜制品表面能生成绿色的铜锈[主要成分为Cu2(OH)2CO3],某化学兴趣小组对铜生锈的条件进行了以下探究。
(提出猜想)根据铜锈的组成元素推测,铜生锈可能是铜与空气中的二氧化碳、水等物质反应的结果。
(实验设计)兴趣小组同学取打磨光量的铜丝,设计了如图所示的四个实验。

(现象分析)若干天后,发现只有D瓶中的铜丝出现绿色的铜锈,其他瓶中的铜丝均无铜锈出现。
(1)实验B、C瓶中所使用的蒸馏水是经煮沸后迅速冷却的蒸馏水,其目的是_____。
(2)B瓶与D瓶中的现象对比,可以得出的结论是_____。
(实验结论)由上述四个实验可分析得出,铜生锈是铜与空气中的_____共同作用的结果。
(拓展探究)以锈蚀严重的废铜屑为原料,回收制取纯铜。查阅资料:Cu2(OH)2CO3+2H2SO4═2CuSO4+3H2O+CO2↑;Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑。如图是该兴趣小组设计的两种回收铜的实验方案:
2CuO+H2O+CO2↑。如图是该兴趣小组设计的两种回收铜的实验方案:

(分析评价)
(3)步骤Ⅲ、Ⅳ、Ⅴ都需要进行的实验操作是_____,该操作中玻璃棒的作用是_____。
(4)步骤Ⅱ过程发生反应的化学方程式为_____,此实验开始时要先通一段时间CO再加热,目的是_____。
(5)同一份废铜屑分别通过上述两种方案最终得到的铜的质量:方案一:_____(填“>”或“=”或“<”)方案二:以上两种方案中,方案二优越于方案一,理由是_____(任答一点)。
【答案】除去水中溶解的二氧化碳和氧气 铜生锈需要二氧化碳 二氧化碳、水蒸气和氧气 过滤 引流 CO+CuO![]() Cu+CO2 排尽空气,防止加热CO和空气的混合物引起爆炸 = 无尾气需要处理,不会污染空气
Cu+CO2 排尽空气,防止加热CO和空气的混合物引起爆炸 = 无尾气需要处理,不会污染空气
【解析】
(1)实验B、C瓶中所使用的蒸馏水是经煮沸后迅速冷却的蒸馏水,其目的是:除去水中溶解的二氧化碳和氧气;故填:除去水中溶解的二氧化碳和氧气;
(2)B瓶与D瓶控制的变量为二氧化碳,通过B瓶与D瓶中的现象对比,可以得出的结论是:二氧化碳是铜生锈的必要条件;故填:铜生锈需要二氧化碳。
[实验结论]由上述四个实验可分析得出,铜生锈是铜与空气中的二氧化碳、水蒸气和氧气共同作用的结果;故填:二氧化碳、水蒸气和氧气。
[分析评价]
(3)步骤Ⅲ、Ⅳ、Ⅴ都需要进行的实验操作是:过滤;在过滤的实验中玻璃棒的作用是引流,故填:过滤;引流。
(4)步骤Ⅱ中,一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,化学方程式为:CO+CuO![]() Cu+CO2;此实验开始时要先通一段时间CO再加热,目的是:排尽空气,防止加热CO和空气的混合物引起爆炸;故 :CO+CuO
Cu+CO2;此实验开始时要先通一段时间CO再加热,目的是:排尽空气,防止加热CO和空气的混合物引起爆炸;故 :CO+CuO![]() Cu+CO2;排尽空气,防止加热CO和空气的混合物引起爆炸。
Cu+CO2;排尽空气,防止加热CO和空气的混合物引起爆炸。
(5)上述两种方案中,铜元素既没有增加,也没有减少,同一份废铜屑分别通过上述两种方案最终得到的铜的质量相等;以上两种方案中,方案二优越于方案一,从环保角度分析其理由是:无尾气需要处理,不会污染空气;故填:=;无尾气需要处理,不会污染空气。


科目:初中化学 来源: 题型:
【题目】南海是我国的固有领海,蕴含着丰富的海洋资源,2017年5月18日,我国南海神狐海域的可燃冰试采取得到圆满成功,实现历史性突破。

(1)可燃冰的主要成分是甲烷,试写出甲烷在空气中燃烧的化学方程式_____。
(2)可燃冰被科学家誉为“未来能源”“21世纪能源”,原因是_____。
(3)1926年我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展.侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠.Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:
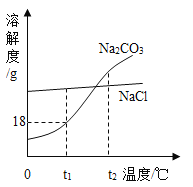
①t1℃时,NaCl的溶解度_____ Na2CO3的溶解度(填“大于”“等于”或“小于”之一);
②t1℃时,50g水中加入10gNa2CO3,经充分溶解,所得溶液中溶质与溶液的质量之比为_____(填最简整数比);
③t1℃时,将不同质量的碳酸钠饱和溶液和氯化钠饱和溶液均升温到t2℃,此时所得碳酸钠溶液溶质质量分数_____ 氯化钠溶液溶质质量分数(填“大于”“等于”或“小于”或“无法判断”之一)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将50克碳酸钙高温煅烧一段时间,冷却后投入足量的稀盐酸中完全反应。下列说法错误的是( )
A.煅烧越充分则消耗盐酸越少
B.整个反应过程中产生的二氧化碳总质量22克
C.煅烧后固体中氧元素质量分数减小
D.反应结束后共生成55.5克氯化钙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图表示元素的化合价与物质类别关系,若它表示氮元素的部分关系图,则下列说法错误的是( )
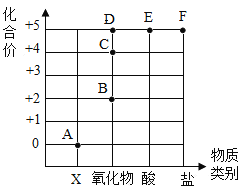
A. A点对应的物质类别是单质
B. B点表示物质的化学式为NO
C. 某化合物的化学式为KNO3,它代表的点是F
D. 写出由D点表示的物质与水发生反应生成E的化学方程式:3NO2+H2O=2HNO3+NO
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于燃烧现象的解释或分析正确的是( )
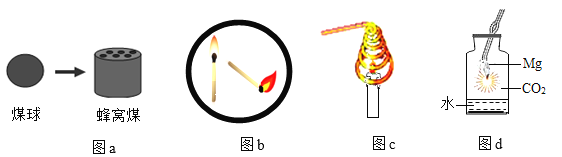
A. 图a中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间
B. 图b中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
C. 图c中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动
D. 由图d中的现象可知,金属镁燃烧的火灾不能用二氧化碳灭火
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E是初中化学常见物质,它们之间的转化关系如图所示。已知:A、B、C均含有人体中含量最高的金属元素,A是氧化物,C、D、E均属于碱,E 为蓝色。
(1)写出化学方程式C→B:____________________。
(2)D 的化学式是:________;
(3)C的一种用途是________。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答:
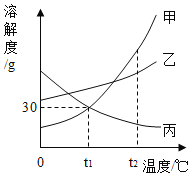
(1)气体的溶解度随温度变化情况与________(选填“甲”“乙”或“丙”)相似。
(2)若乙中混有少量的甲,最好采用________的方法提纯乙。
(3)t1℃时,向盛有15g丙物质的烧杯中加入50 g水,充分溶解后得到65 g溶液。若要增大该溶液的溶质质量分数,可采用的方法是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关测定氢氧化钠溶液pH的实验操作或描述,你认为正确的是( )
A. 用镊子夹取pH试纸直接伸入氢氧化钠溶液中测量
B. 先用蒸馏水将pH试纸润湿,再用滴管吸取氢氧化钠溶液滴到pH试纸上测量
C. 用洁净干燥的玻璃棒蘸取氢氧化钠溶液滴到pH试纸上,再与标准比色卡对照
D. 用pH试纸测得该氢氧化钠溶液的![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧化锌软膏可用于急性或亚急性皮炎、湿疹、痱子及轻度、小面积的皮肤溃疡。闪锌矿(主要成分为ZnS)是含锌的主要矿物质之一,高温煅烧闪锌矿生成氧化锌和SO2,以氧化锌产品为原料制备纯氧化锌的生产工艺流程如图:
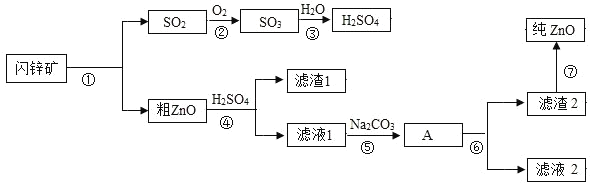
(1)已知滤液2主要成分是硫酸钠,则滤渣2的化学式为_____。
(2)上述步骤中,步骤⑥的操作是_____(填操作名称)。此操作中用到的玻璃仪器有烧杯,玻璃棒、_____。
(3)步骤④的反应,基本类型是_____反应。
(4)步骤④中,若选用的稀硫酸溶质的质量分数为9.8%,则用100mL98%的浓硫酸(密度为1.8g/cm3)配制该稀硫酸,需加水_____g。
(5)步骤②③两步反应,可以写成一个总的化学反应的化学方程式,该总反应的化学方程式是_____ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com