
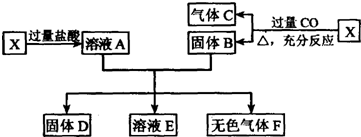
分析 此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,根据叙述的关键,以及物质的性质和物质之间的反应,做出判断,X为氧化亚铁与氧化铜的混合物,与过量的盐酸反应形成的溶液A含有盐酸,与过量一氧化碳反应生成的固体B含有铁和铜,固体A和B反应的到了固体D和溶液E,则D中含有铜,溶液E含有氯化亚铁,所得固体D的质量为16g,溶液E中含有盐酸和一种盐,则铁全部参加反应,D为铜,E中含有氯化亚铁和盐酸,根据题干提供的据以及反应的化学方程式进行计算即可.
解答 解:(1)固体D的质量是Fe和CuCl2溶液反应生成的Cu和CO还原氧化铜生成的Cu的总质量,即两份X样品中铜元素的总质量,所以,每份样品中铜元素的质量为8g.每份样品中氧化铜的质量为:8g÷64×80=10g,设与盐酸反应的铁的质量为x
5.6L氢气的质量为:5.6L×5/56g/L0.5g
Fe+2HCl═FeCl2+H2↑
56 2
x 0.5g
$\frac{56}{x}$=$\frac{2}{0.5g}$
x=14g
设与CuCl2反应的铁的质量为y
Fe+CuCl2=FeCl2+Cu
56 64
y 8g
$\frac{56}{y}$=$\frac{64}{8g}$
y=7g
每份X样品中铁元素的质量为:14g+7g=21g
每份X样品中氧化亚铁的质量为:
21g÷($\frac{56}{72}$×100%)=27g
因此,每份X样品中氧化亚铁和氧化铜的质量比为:27g:10g=27:10;
故答案为:取用的每份X中氧化亚铁与氧化铜的质量比为27:10;
(2)氧化亚铁和氧化铜的“分子”个数比为:$\frac{27g}{72}$:$\frac{10g}{80}$=3:1,每份X中铁原子和氧原子的个数比为:3:(3+1)=3:4
答:每份X中氧化亚铁与氧化铜的质量比为27:10,每份X中铁与氧的原子个数比为3:4.
点评 本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式,根据方程式进行计算时,要找准参加反应的物质的质量.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:初中化学 来源: 题型:选择题
| A. | 氯化钾溶液和硝酸 | B. | 氢氧化钡溶液和硫酸 | ||
| C. | 碳酸氢钡溶液和硫酸 | D. | 硫酸镁溶液和氢氧化钾溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 它是一种复合肥 | |
| B. | 它是无机化合物 | |
| C. | 它由氮、氢、碳、氧四种元素组成 | |
| D. | 它的组成中氮原子和氢原子的个数比是1:5 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①Ca(OH)2 ②CaO ③SO3 ④CaSO4 ⑤CaCO3 | |
| B. | ①CaO ②Ca(OH)2 ③CO ④CaSO4 ⑤CaCO3 | |
| C. | ①CaCO3 ②CaO ③CO2 ④Ca(OH)2 ⑤CaCO3 | |
| D. | ①CaCO3 ②CaO③SO2 ④CaSO4 ⑤Ca(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 21% | B. | 32% | C. | 37% | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com