
���� ��1�����ݻ������и�Ԫ��������=��ԭ�ӵ����ԭ��������ԭ�Ӹ���֮�ȣ����з������
��2���������⣬ij��ʯ���к���������74%������Ϊ���ʣ��ɵ�ʯ�����������������ʯ�����������Ƶ��������ɣ�
��3�������Է�ˮ����������������ݷ�Ӧ�Ļ�ѧ����ʽ�����������Ҫ��ʯ�����������ɣ�
��� �⣺��1����Ȳ��̼����Ԫ�ص�������Ϊ��12��2������1��2��=12��1��
��2��100kg������ʯ�����������Ƶ�����Ϊ100kg��74%=74kg��
��3����������Ҫ��ʯ��������Ϊx
Ca��OH��2+H2SO4�TCaSO4+2H2O
74 98
74%•x 196kg
$\frac{74}{74%•x}$=$\frac{98}{196kg}$
��ã�x=200kg
��������Ҫ��ʯ��������Ϊ200kg��
�ʴ�Ϊ��
��1��12��1��
��2��74��
��3��200kg��
���� �����ѶȲ������ո��ݻ�ѧ����ʽ�ļ��㡢��ѧʽ���йؼ��㼴����ȷ����⣬����ʱҪע�����Ĺ淶�ԣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��H-O-��-O-O-���ȼ��֣�����Ϊ�����ط�������ɱ�����õ�ԭ�Ӽ����ϵķ�ʽ��-O-O-����������������֪ʶ���е������������Ƿ���ȷ����Ҫͨ��ʵ�������֤��
��H-O-��-O-O-���ȼ��֣�����Ϊ�����ط�������ɱ�����õ�ԭ�Ӽ����ϵķ�ʽ��-O-O-����������������֪ʶ���е������������Ƿ���ȷ����Ҫͨ��ʵ�������֤���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10mL�ƾ���10mLˮ��Ϻ����С��20mL������Ϊ���ӱ�С�� | |
| B�� | �����к������������ǵ��� | |
| C�� | �����г�����еķ�����Ӳˮת��Ϊ��ˮ | |
| D�� | ����ɭ�ֻ���ʱ���ɿ��ڷ�����������Ŀ���Ǹ����ȼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
 ��ͼ�Ǽס������ֹ�����ܽ�����ߣ�����˵����ȷ���ǣ�������
��ͼ�Ǽס������ֹ�����ܽ�����ߣ�����˵����ȷ���ǣ�������| A�� | ���ܽ�ȴ����ҵ��ܽ�� | |
| B�� | 10��ʱ���ס��ұ�����Һ������������� | |
| C�� | 20��ʱ����10g�����ʼ���50gˮ�У��õ�60g��Һ | |
| D�� | ���л����������ң��ᴿ�ײ��ý��½ᾧ�ķ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
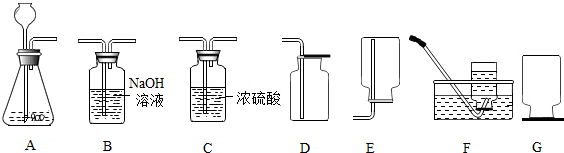
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
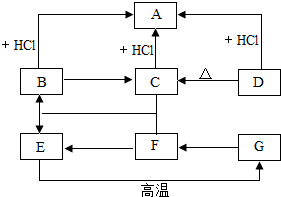 ��ͼΪ��ѧ��ѧ�г��������ʣ�A��B��C��D���Ǻ�����Ԫ�صĻ����2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2������E��F��GΪ���и�Ԫ�صĻ����ͼ�С�-����ʾ���˵������ܷ�����ѧ��Һ����������ʾ����֮�����ת����ϵ��
��ͼΪ��ѧ��ѧ�г��������ʣ�A��B��C��D���Ǻ�����Ԫ�صĻ����2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2������E��F��GΪ���и�Ԫ�صĻ����ͼ�С�-����ʾ���˵������ܷ�����ѧ��Һ����������ʾ����֮�����ת����ϵ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ������ | C�� | ���������� | D�� | ���Ӳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
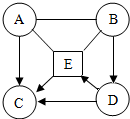 ��֪A��B��C��D��E��Ϊ���л�ѧ�������ᡢ��Σ�����A������Ԫ����ɣ�B��D���Ǽ���B����ˮ��C��������ˮ����ɳɷ֣�E�����ڲ�������ֽ����֯�����û�ѧ��ҵ�������������Һ������ͼ��ʾ��ת����ϵ����֪A��E�ܷ�Ӧ�������壬��ش��������⣮����-����ʾ����ܷ�Ӧ����������ʾ��ij�������������ɸ����ʣ�
��֪A��B��C��D��E��Ϊ���л�ѧ�������ᡢ��Σ�����A������Ԫ����ɣ�B��D���Ǽ���B����ˮ��C��������ˮ����ɳɷ֣�E�����ڲ�������ֽ����֯�����û�ѧ��ҵ�������������Һ������ͼ��ʾ��ת����ϵ����֪A��E�ܷ�Ӧ�������壬��ش��������⣮����-����ʾ����ܷ�Ӧ����������ʾ��ij�������������ɸ����ʣ��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com