
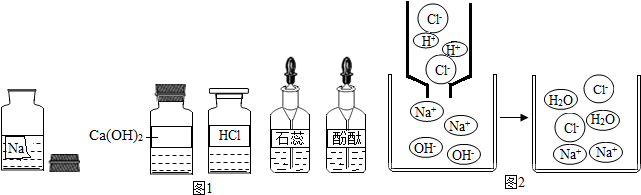
分析 【实验推断】(1)根据氯化钠、氢氧化钠、碳酸钠三种溶液的酸碱性进行分析;
(2)根据碳酸钠溶液与盐酸的反应进行分析;
(3)根据氢氧化钠与空气中二氧化碳反应进行分析;
【继续探究】根据碳酸钠和氯化钙反应结合碳酸钠和氢氧化钠的检验方法进行分析;
【实验结论】根据实验现象得出结论;
【探究启示】根据结论分析保存方法.;
【拓展迁移】根据反应的微观示意图结合反应的实质分析.
解答 解:【实验推断】
(1)氢氧化钠和碳酸钠溶液都呈碱性能使酚酞试液变红色,氯化钠溶液呈中性,所以,小丽取样滴加无酚酞试液,溶液呈红色,得出结论:该溶液不可能是氯化钠溶液;故填:NaCl溶液呈中性,不能使无色酚酞试液变红;
(2)若有碳酸钠存在,滴加盐酸,发生反应Na2CO3+2HCl=2NaCl+H2O+CO2↑,有气泡产生.所以,小刚另取样滴加稀盐酸有气泡产生,小刚得出结论:该溶液是碳酸钠溶液;故填:气体;Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)因为该试剂是敞口放置于空气中,若是氢氧化钠可能会和空气中二氧化碳反应变质生成部分碳酸钠,所以,小青认为小刚的结论不完全正确,理由是露置于空气中的NaOH溶液与空气中的CO2反应也生成碳酸钠;故填:NaOH溶液变质后滴加稀盐酸也会产生气体;
【继续探究】要证明原来是氢氧化钠,可先加过量氯化钡或氯化钙溶液溶液除尽碳酸根,再用酚酞检验氢氧化钠的存在.所以,另取样加入过量的CaCl2溶液,观察到有白色沉淀产生,设计这一步骤的目的是完全除去溶液中的CO32-,避免其对OH-检验造成干扰;静置后,取上层清液,滴入酚酞试液,溶液呈红色;故填:白色沉淀;
除去Na2CO3防止干扰;
【实验结论】因为滴加氯化钙有白色沉淀产生且滴加酚酞变红色,说明含有碳酸钠和氢氧化钠;故填:NaOH和Na2CO3;
【拓展迁移】通过观察反应的微观过程图,可以看出反应后溶液的阴阳离子为Cl-、Na+;故填:Cl-、Na+.
点评 本题是缺失标签的实验探究题,相当于物质鉴别题,在鉴别几种物质时要从物质的不同性质入手,但试题涉及知识点多,要加强知识的全面性和系统性.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:初中化学 来源: 题型:选择题
| A. | 学生营养餐提供牛奶、馒头、蔬菜等 | |
| B. | 用棉花和某些合成纤维制衣服等 | |
| C. | 用甲醛或硝酸汞溶液浸泡海产品 | |
| D. | 青少年适当食用含钙、铁化合物的保健品来补充人体所需的钙、铁元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量A溶液于试管中,向其中滴加酚酞溶液 | 酚酞溶液变红色 | 假设①正确. 碳酸钠与其反应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH. |

| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气体产生 | 猜想不成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
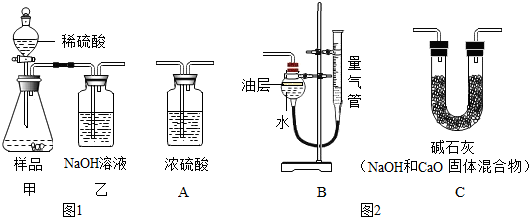
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用篮子代替塑料袋 | B. | 提倡使用一次性筷子 | ||
| C. | 使用节能灯泡 | D. | 节约每一滴水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Mg | B. | CO2 | C. | MgO | D. | C |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com