
【题目】已知A、B为两种黑色粉末,D为红色单质。A、B、C、D、E五种物质之间的转化关系如下图所示。请回答:
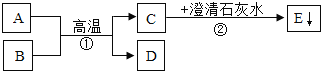
(1)C的化学式为_____;
(2)标出A中金属元素化合价____;
(3)反应①的化学方程式为_____;该反应的基本类型是_____。
(4)反应②的化学方程式为_______。
【答案】CO2 ![]()
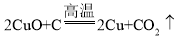 置换反应
置换反应 ![]()
【解析】
A、B为两种黑色粉末,D为红色单质,A、B在高温的条件下反应生成C和D,氧化铜和碳都是黑色,且氧化铜能与碳在高温的条件下反应生成铜和二氧化碳,铜为红色,可推出A、B为氧化铜和碳,C为二氧化碳,D为铜;二氧化碳可与氢氧化钙反应生成碳酸钙和水,故E为碳酸钙。
(1)C为二氧化碳,化学式为:CO2;
(2)标出A中金属元素化合价,则A为氧化铜,铜通常为+2价,元素化合价的表示方法是在化学式该元素的上方用正负号和数字表示,正负号标在数字前面,故标出A中金属元素化合价为:![]() ;
;
(3)反应①为氧化铜和碳在高温的条件下反应生成铜和二氧化碳,该反应的化学方程式为: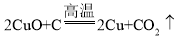 ,该反应符合“一种单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应;
,该反应符合“一种单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应;
(4)反应②为二氧化碳与氢氧化钙反应生成碳酸钙和水,该反应的化学方程式为:![]() 。
。


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:初中化学 来源: 题型:
【题目】在奥运比赛中,举重运动员举重前常用白色的“镁粉”搓手,是因为“镁粉”质轻、吸水性好,可作防滑剂.“镁粉”的有效成分是碱式碳酸镁,它不可燃,300℃即分解,其分解的化学方程式是:Mg5(OH)2(CO3)4![]() 5MgO+X+4CO2↑,则X的化学式是( )
5MgO+X+4CO2↑,则X的化学式是( )
A. O2 B. CO C. Mg(OH)2 D. H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室现有一瓶含少量水的碳酸氢铵样品,为测定其中碳酸氢铵的质量分数,某化学兴趣小组利用如图所示装置进行实验(该装置气密性良好,装置B、C中所装药品均足量,碱石灰是氧化钙和氢氧化钠的混合物)。已知:NH3能被酸溶液吸收。
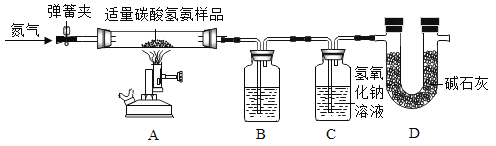
部分实验步骤如下:
Ⅰ、打开弹簧夹,通入一段时间的氮气;
Ⅱ、关闭弹簧夹,给碳酸氢铵样品加热;
Ⅲ、当样品反应完全,…,再停止加热,直到玻璃管冷却;
Ⅳ、实验完毕,测得装置B、C中药品的质量分别增加了m1、m2。
请回答下列问题:
(1)氨气溶于水显_____(填“酸性”、“中性”或“碱性”)。NH4HCO3属于_____(选填“氮肥”“磷肥”“钾肥”或“复合肥”),该物质中氮元素的化合价为_____。
(2)装置B中盛放的液体是_____。装置C中发生反应的化学方程式为_____,装置D的作用是_____。
(3)步骤Ⅲ中,当样品反应完全时的现象是_____,停止加热前应进行的操作是_____。
(4)该样品中碳酸氢铵的质量分数的表达式为_____(用m1、m2的代数式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是初中化学课堂中出现的装置,请据图回答:
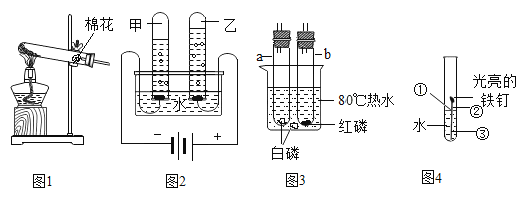
(1)四个图中均含有同一种仪器,它的名称是_______________.
(2)写出图1中发生反应的化学方程式__________________
(3)由图2可以得出的实验结论是__________
(4)图3中a试管装有白磷和空气、b试管装有红磷和空气,烧杯中盛有80℃热水,底部有一小块白磷,可以得出“可燃物燃烧需要氧气”的实验对比现象是_______________
(5)图4实验中铁钉最易生锈的部位是________(填①、②或③)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图所示为实验室中常见的气体制备和收集装置。
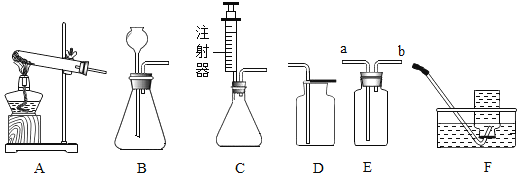
(1)实验室用加热氯酸钾和二氧化锰的混合物制取氧气,应选用发生装置________(填字母序号),反应的文字表达式为_______。试管口略向下倾斜的原因是____实验结束后,应先________,再 _______,防止_____。
(2)若用F装置收集氧气,____________ 开始收集,_______证明收集满了。若用装置D收集氧气,验满的方法是_________________。
(3)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用B做发生装置,加入药品前应先________具体做法是_________若选用C做发生装置,你认为选用C的优点是________。
(4)欲使用装置E用排空气法收集氧气,则气体应从______(填“a”或“b”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从______(填“a”或“b”)端通入。
(5)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置________(填字母序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一氧化碳和二氧化碳是碳元素的两种重要化合物。
(1)从组成上看它们的相同点是__________。
(2)其中可用于冶炼金属的是________。
(3)写出二氧化碳转化成一氧化碳的化学方程式__________。
(4)根据化学方程式计算:11.2g的一氧化碳完全燃烧,生成二氧化碳的质量是多少?________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】了解物质的组成和结构,有助于认识物质的性质。
(1)下图表示核电荷数为11~17元素的最高和最低化合价。

①从图中可以看出,氯元素的最高正价是____。
②若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为____。
③写出图中元素的化合价随着核电荷数递增的一条变化规律:____。
(2)在金属活动性顺序表里,通常排在前面的金属更易失去电子。回答以下问题:
①某金属原子的结构示意图为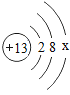 ,则最外层电子数x=______;若最外层电子失去,达到相对稳定结构,该带电粒子的符号为_____。
,则最外层电子数x=______;若最外层电子失去,达到相对稳定结构,该带电粒子的符号为_____。
②我国古代发明了“曾青(即硫酸铜)得铁化为铜”的湿法炼铜法,将铁放入硫酸铜溶液中可以生成铜和硫酸亚铁,写出该反应的符号表达式:____,反应中,更易失去电子的金属是___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对比试验是最基本的科学分析方法,请根据下图A﹣F组试验,完成下表实验设计.
实验序号 | 探究目的 | 选用对比实验(填组序号) |
1 | 不同的温度,对分子运动的影响 | __ |
2 | __ | C组 |
3 | 干燥的CO2能否使石蕊变红 | __ |
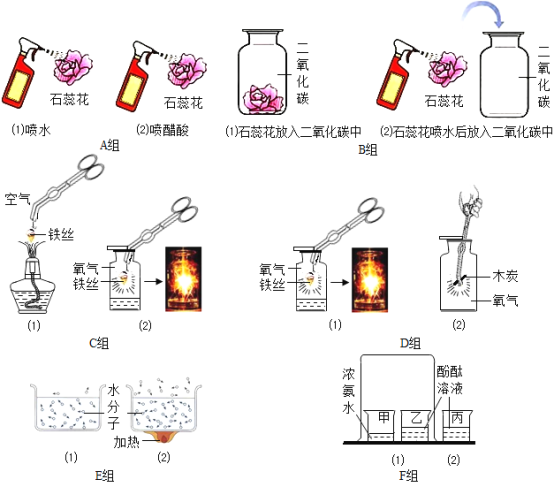
查看答案和解析>>
科目:初中化学 来源: 题型:
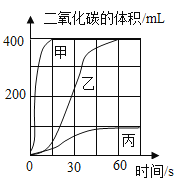
【题目】实验室制备并收集二氧化碳,按下表进行实验。取等质量的同种大理石加入足量酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如图所示。下列说法错误的是
实验编号 | 药品 |
Ⅰ | 块状大理石、10% H2 SO4溶液 |
Ⅱ | 块状大理石、7% HCl溶液 |
Ⅲ | 大理石粉末、7% HCl溶液 |
A.实验Ⅲ对应的左图变化曲线为甲
B.实验II和Ⅲ对比,说明影响反应速率的因素是固体的颗粒大小
C.实验I和Ⅱ对比,说明影响反应速率的因素是酸的浓度
D.实验Ⅱ和Ⅲ完全反应后,产生二氧化碳的质量是相等的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com