
分析 (1)碘酒中的溶质是碘,溶剂是酒精;
(2)酸具有相似的化学性质,是因为酸中都能解离出相同的氢离子;
通常人体胃液中的酸主要是稀盐酸,稀盐酸和氢氧化铝反应生成氯化铝和水;
(3)生石灰放在空气中变质,这是因为它会和空气中的水蒸气发生反应生成氢氧化钙;
如果不及时处理该反应的生成物会继续与空气中的CO2发生反应生成碳酸钙和水;
(4)四氧化三铁和一氧化碳在高温条件下反应生成铁和二氧化碳;
当铁在放置久了会生锈,是因为它与空气中的水和氧气发生了反应,铁锈的主要成分是氧化铁,因为铁锈疏松多孔,如果不及时处理会使铁钉完全锈蚀,在铁制品表面涂一层油漆可以防止生锈;
一枚生锈的铁钉放在稀盐酸中除铁锈,氧化铁和稀盐酸反应生成氯化铁和水;
铁和稀盐酸反应生成氯化亚铁和氢气;
(5)天然气的主要成分是甲烷,甲烷燃烧生成水和二氧化碳;
灭火的方法有:移走可燃物,隔绝氧气,降低温度到可燃物的着火点以下;
通常情况下,锌和稀硫酸反应生成硫酸锌和氢气;
氢气燃烧生成水,不污染环境;
化石燃料日趋枯竭,开发利用新能源具有重要意义,人类正在开发利用的新能源有太阳能、核能、风能、水能、地热能、潮汐能、氢能等.
解答 解:(1)碘酒中的溶质是I;溶剂是C2H5OH.
故填:I;C2H5OH.
(2)酸具有相似的化学性质,是因为酸中都能解离出相同的H+,通常人体胃液中的酸主要是HCl,如果胃酸过多会使人胃疼,为了缓解胃痛人们常服用斯达舒来缓解,其主要成分是Al(OH)3,它在人体当中发生的化学反应方程式为:Al(OH)3+3HCl═AlCl3+3H2O.
故填:H+;HCl;Al(OH)3; Al(OH)3+3HCl═AlCl3+3H2O.
(3)生石灰放在空气中变质,这是因为它会和空气中的水蒸气发生反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2;
如果不及时处理该反应的生成物会继续与空气中的CO2发生反应生成碳酸钙和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:CaO+H2O═Ca(OH)2;Ca(OH)2+CO2═CaCO3↓+H2O.
(4)四氧化三铁和一氧化碳在高温条件下反应生成铁和二氧化碳,反应的化学方程式为:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;
当铁在放置久了会生锈,是因为它与空气中的H2O和O2发生了反应,铁锈的主要成分是Fe2O3,涂一层油漆可以防止铁制品生锈;
一枚生锈的铁钉放在稀盐酸中除铁锈,氧化铁和稀盐酸反应生成氯化铁和水,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;
铁和稀盐酸反应生成氯化亚铁和氢气,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故填:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;H2O;O2;Fe2O3;涂一层油漆;Fe2O3+6HCl═2FeCl3+3H2O;Fe+2HCl═FeCl2+H2↑.
(5)天然气的主要成分是甲烷,甲烷燃烧生成水和二氧化碳,反应的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
如果不慎发生火灾,消防员会利用高压水枪将火熄灭,其原理是降低温度至可燃物着火点以下;
实验室制取氢气的化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
氢气是最清洁的燃料,是因为氢气燃烧生成水,不污染环境,反应的化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
人类正在开发的新能源有核能、太阳能等.
故填:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;降低温度至可燃物着火点以下;Zn+H2SO4═ZnSO4+H2↑;2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;核能.
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较小.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70 | 70 | 70 | 70 |
| 剩余固体质量/g | 18.2 | 16.4 | 14.6 | 13.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 如果不慎将浓硫酸沾在皮肤上,应立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液 | |
| B. | 如果不小心将酒精灯打翻而造成酒精在桌面上燃烧起来,应立即用湿抹布扑盖 | |
| C. | 如果不慎将氢氧化钠溶液沾在皮肤上,应立即用大量的水冲洗,再涂上硼酸溶液 | |
| D. | 如果因胃酸过多而引起的胃不适,可以喝一些稀氢氧化钠溶液加以中和 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
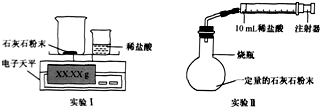 某校学习小组准备探究气体的测定和数据处理方法.
某校学习小组准备探究气体的测定和数据处理方法.| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com