
分析 (1)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得苹果酸钠盐的相对分子质量为:12×4+5+16×5+23=156.故填:156;
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得苹果酸钠盐中碳、氧元素的质量比为(12×4):(16×5)=3:5.故填:3:5;
(3)312g苹果酸钠盐中钠元素的质量是:312g×$\frac{23}{156}×100%$=46g;故填:46g.
点评 本题难度不大,考查同学们灵活运用所学化学式的有关计算进行解题的能力.


 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
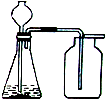
| A. | 用KMnO4粉末制取O2 | |
| B. | 用KClO3和MnO2制取O2 | |
| C. | 用Zn(固体)和稀硫酸制(液体)取H2 (密度比空气小,难溶于水) | |
| D. | 用石灰石(固体)和稀盐酸(液体)制取CO2(密度比空气大,溶于水) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
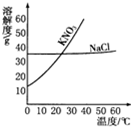 根据如图中KNO3和NaCl的溶解度曲线,回答下列问题.
根据如图中KNO3和NaCl的溶解度曲线,回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

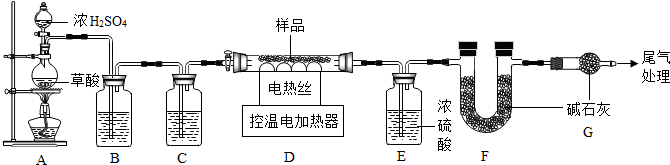
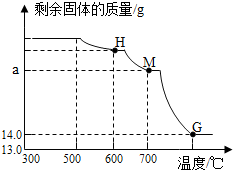
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 谷氨酸钠相对分子质量为169 | |
| B. | 谷氨酸钠是由5个碳原子、8个氢原子、4个氧原子、1个氮原子和1个钠原子构成 | |
| C. | 20℃时,100g水最多可配制成171.7g谷氨酸钠的饱和溶液 | |
| D. | 谷氨酸钠中钠元素的质量分数约为13.6% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com