
| A. | 生成2.0 gCO2气体 | B. | 原来CaCO3的质量为14.3 g | ||
| C. | 生成了5.6 gCaO | D. | 剩余CaCO3的质量为3.0 g |
分析 由于加热过程中生成二氧化碳,所以固体中的钙元素质量保持不变,所以可以根据钙元素进行相关计算.
解答 解:由于剩余固体质量为8.0g,而其中的钙元素质量分数为50.0%,则对应钙元素质量为8.0g×50.0%=4.0g,则对应的原来的碳酸钙的质量为4.0g÷($\frac{40}{40+12+16×3}×100%$)=10.0g,则生成的二氧化碳的质量为10.0g-8.0g=2.0g.则反应掉的碳酸钙质量为x,生成氧化钙质量为y.
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
100 56 44
x y 2.0g
$\frac{100}{x}$=$\frac{56}{y}$=$\frac{44}{2.0g}$
x≈4.55g y≈2.55g
剩余碳酸钙的质量为10.0g-4.55g=5.45g
所以只有A选项是正确的.
故选:A.
点评 在审题中抓住钙元素质量保持不变即可,进行其余对应物质的计算.


科目:初中化学 来源: 题型:实验探究题
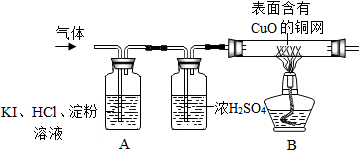
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
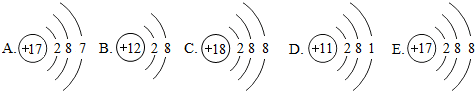
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用液态二氧化碳灭火器扑灭图书档案室的火灾 | |
| B. | 稀盐酸可以用来除铁锈 | |
| C. | 用氮气作为灯泡填充气 | |
| D. | 面团发酵会产生酸味,可以添加烧碱中和 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
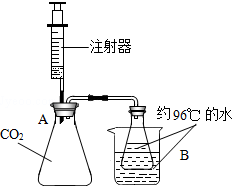 CO2是一种宝贵的碳氧资源.
CO2是一种宝贵的碳氧资源.查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 不显电性 | B. | 相当于一个氦(He)原子的质量 | ||
| C. | 失去一个中子后显+1价 | D. | 在周期表中与氢元素占同一位置 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com