

分析 (1)溶液稀释时溶质的质量不变,注意稀释浓硫酸的方法.
(2)①掌握氢氧化钠变质的原因;
②根据氢氧化钠的特点考虑:氢氧化钠易与空气中二氧化碳反应生成碳酸钠,加入的物质与碳酸根离子能产生气体,来考虑加入的物质;
③过量的CaCl2溶液与碳酸钠反应,把碳酸钠全部消耗,再考虑加入酚酞变色情况.氢氧化钠变质是与二氧化碳反应导致.
(3)根据晒盐的原理分析即可;根据氢氧化钠会而会和氯化镁反应生成沉淀进行分析
(4)反应后所得溶液是氯化钠溶液,根据化学方程式NaOH+HCl=NaCl+H2O,可以计算生成氯化钠的质量,最后用氯化钠的质量除以所得溶液的质量乘以百分之百便可得反应后所得溶液中溶质的质量分数.
解答 解:(1)溶液在稀释时溶质的质量不变,
需加水的质量为x,则
10g×98%=(10g+x)×20%
解得:x=39g
浓硫酸溶于水放出大量的热,并且浓硫酸的密度比水的大,所以在稀释浓硫酸时应该将浓硫酸慢慢注入水中,同时要不断的搅拌,使产生的热量及时散失.
(2)①氢氧化钠变质的原因是氢氧化钠与空气中的二氧化碳反应,则化学方程式为 2NaOH+CO2═Na2CO3+H2O;
②氢氧化钠易与空气中二氧化碳反应生成碳酸钠,由于碳酸根遇到酸能产生气体二氧化碳,所以加入的物质是盐酸就行;
③氢氧化钠变质后有两种情况:全变质,部分变质,全变质就是全部为碳酸钠,部分变质是既有氢氧化钠也有碳酸钠,过量的CaCl2溶液把碳酸钠全部反应掉,再加入酚酞变红,说明显碱性溶液中含有氢氧化钠,所以部分变质;
(3)从海水中提取食盐采用蒸发结晶的方法,风吹日晒是为了加速水分的蒸发;所有的钠盐都溶于水,而氢氧根离子会将镁离子转化为氢氧化镁沉淀,剩余氯化钠;
(4)设反应生成的NaCl的质量为x.
NaOH+HCl═NaCl+H2O
36.5 58.5
73g×20% x
$\frac{36.5}{73g×20%}=\frac{58.5}{x}$,
解得x=23.4g
所以反应后所得溶液中溶质的质量分数为$\frac{23.4g}{73g+127g}$×100%=11.7%
答:反应后所得溶液中溶质的质量分数为11.7%.
故答案为:(1)39;将浓硫酸沿着器壁慢慢倒入水中,并用玻璃棒不断搅拌,使产生的热量迅速散失;
(2)①2NaOH+CO2═Na2CO3+H2O;②稀盐酸; ③部分;
(3)蒸发除去水分;氢氧化钠;(4)11.7%.
点评 解答本题要注意变质后的溶液不能直接用酚酞溶液来判断,因为变质后的碳酸钠也显碱性;还考查根据化学方程式计算和溶质质量分数的计算,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:推断题
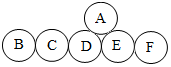 A、B、C、D、E、F分别是氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液、一氧化碳、二氧化碳中的一种.他们之间有如图所示的反应关系,图中相连的两圆表示相应物质间能发生反应,固态C物质可用于人工降雨.回答下列问题:
A、B、C、D、E、F分别是氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液、一氧化碳、二氧化碳中的一种.他们之间有如图所示的反应关系,图中相连的两圆表示相应物质间能发生反应,固态C物质可用于人工降雨.回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 萘胺中含有20个原子 | B. | 萘胺中氮元素的质量分数约为9.7% | ||
| C. | 二氧化钛和萘胺都是有机物 | D. | 这种试纸是一种新型化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 杂质 | 除杂质应选用的试剂和操作方法 | |
| A | CO2 | CO | 通入O2,点燃 |
| B | 铁粉 | 铜粉 | 加入适量盐酸,过滤 |
| C | KNO3溶液 | KOH溶液 | 加入适量的CuSO4溶液,过滤 |
| D | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 熟石灰不能与氯化铵混合施肥 | |
| B. | 食品包装中不能用烧碱做干燥剂 | |
| C. | 常用钢丝球擦洗铝壶可以使其光亮洁净和更耐用 | |
| D. | 通常用含单质碳的墨水书写档案,以便于长期保存 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | XZYW | B. | ZXYW | C. | WYXZ | D. | WYZX |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生石灰 CaO 做干燥剂 | |
| B. | 纯碱 NaOH 治疗胃酸过多 | |
| C. | 小苏打 NaHCO3发酵粉主要成分之一 | |
| D. | 干冰 CO2人工降雨 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com