
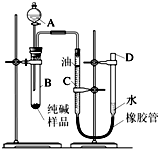
 小沁同学用如图所示装置测定某纯碱样品(杂质为NaCl)中Na2CO3的质量分数.C为有刻度的玻璃仪器,可装合适的液体,根据液面位置变化测定气体体积.
小沁同学用如图所示装置测定某纯碱样品(杂质为NaCl)中Na2CO3的质量分数.C为有刻度的玻璃仪器,可装合适的液体,根据液面位置变化测定气体体积.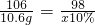 x=98g
x=98g

科目:初中化学 来源: 题型:
 小沁同学用如图所示装置测定某纯碱样品(杂质为NaCl)中Na2CO3的质量分数.C为有刻度的玻璃仪器,可装合适的液体,根据液面位置变化测定气体体积.
小沁同学用如图所示装置测定某纯碱样品(杂质为NaCl)中Na2CO3的质量分数.C为有刻度的玻璃仪器,可装合适的液体,根据液面位置变化测定气体体积.查看答案和解析>>
科目:初中化学 来源: 题型:
 (2012?高淳县一模)小沁同学用如图所示装置测定某纯碱样品(杂质为NaCl)中Na2CO3的质量分数.C为有刻度的玻璃仪器,可装合适的液体,根据液面位置变化测定气体体积.
(2012?高淳县一模)小沁同学用如图所示装置测定某纯碱样品(杂质为NaCl)中Na2CO3的质量分数.C为有刻度的玻璃仪器,可装合适的液体,根据液面位置变化测定气体体积.查看答案和解析>>
科目:初中化学 来源:2012年江苏省泰州市姜堰二附中中考化学二模试卷(解析版) 题型:填空题
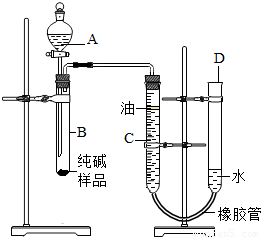
查看答案和解析>>
科目:初中化学 来源:2012年江苏省南京市高淳县中考化学一模试卷(解析版) 题型:解答题
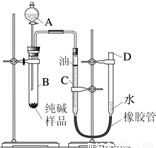
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com